Тиотропия бромид. Тиотропия бромид (Tiotropium bromide) Тиотропия бромид обладает следующими свойствами
Состав
1 капсула содержит:
Активный ингредиент: 22,5 мкг тиотропия бромида моногидрата, эквивалентно 18 мкг тиотропия.
Вспомогательные вещества: лактозы моногидрат 200 М; лактозы моногидрат микронизированный.
Состав капсулы: желатин, полиэтиленгликоль, индигокармин (Е 132), титана диоксид (Е 171), железа оксид желтый (Е 172).
Описание
Твердые желатиновые капсулы, размер 3, светло-зеленовато-голубого цвета, непрозрачные, с надпечаткой символа компании и TI 01 черными чернилами. Содержимое капсул - белый порошок.
Фармакотерапевтическая группа
Прочие средства ингаляционного применения для лечения обструктивных заболеваний дыхательных путей. Антихолинергические средства. Код АТХ: R03BB04.
Фармакологические свойства
Фармакодинамика
Механизм действия
Тиотропия бромид - специфический антагонист мускариновых рецепторов длительного действия. Связываясь с мускариновыми рецепторами гладкой мускулатуры бронхов, тиотропия бромид блокирует холинергические (бронхоконстрикторные) эффекты ацетилхолина, высвобождаемого из парасимпатических нервных окончаний. Он обладает сходным сродством к М1-М5 подтипам мускариновых рецепторов. В дыхательных путях тиотропия бромид конкурентно и обратимо связывается с М3-рецепторами гладкой мускулатуры бронхов, что приводит к снижению тонуса гладкой мускулатуры и бронходилатации. Эффект является дозозависимым и сохраняется более 24 часов. Длительность действия, вероятно, связана с очень медленной диссоциацией связи с М3 рецептором, что отражено в достоверно более длительном периоде полураспада, чем у ипратропия. Являясь N-четвертичным холиноблокатором, тиотропия бромид при ингаляционном введении оказывает местное селективное действие на бронхи, демонстрируя приемлемый терапевтический диапазон доз без возникновения системных антихолинергических эффектов.
Фармакодинамические эффекты
Бронходилатирующий эффект преимущественно локальный без системного действия. В исследовании in vitro установлено более быстрое высвобождение тиотропия из связи с М2-рецепторами, чем из связи с М3-рецепторами, что приводит к фармакокинетически обусловленному селективному действию препарата в отношении М3 подтипа рецепторов по сравнению с Мг подтипом. Высокая активность, очень медленное высвобождение из связи с рецептором и местное селективное действие при ингаляционном введении приводит к клинически достоверному длительному бронходилатирующему действию тиотропия у пациентов с ХОБЛ.
Электрофизиология сердца
В специально проведенных исследованиях влияния препарата на интервал QT с участием 53 здоровых добровольцев СПИРИВА, принимаемая в дозах 18 мкг и 54 мкг (т.е. в три раза выше терапевтической дозы) в течение 12 дней, не вызывала достоверного удлинения интервала QT на ЭКГ.
Клиническая эффективность и безопасность
Программа клинических исследований включала четыре одногодичных, два 6- месячных рандомизированных двойных слепых исследования с участием 2663 пациентов (из них 1308 пациентов получали тиотропий). 1-летняя программа состояла из двух плацебо-контролируемых исследований и двух исследований с активным контролем (ипратропий). Оба шестимесячных исследования проходили с контролем салметеролом и плацебо. Все исследования включали изучение влияния препарата на функцию легких и исходы влияния на одышку, обострения и связанное со здоровьем качество жизни.
Функция легких
Тиотропия бромид, применяемый один раз в сутки, обеспечивал достоверное улучшение функции легких (объема форсированного выдоха за одну секунду (ОФВ1) и форсированной жизненной емкости легких (ФЖЕЛ)) в течение 30 минут после ингаляции первой дозы, при этом действие сохранялось в течение 24 часов. Фармакодинамическое равновесное состояние достигалось в течение одной недели с максимальной бронходилатацией с третьего дня приема. При использовании тиотропия бромида достоверно повышалась пиковая скорость выдоха (ПСВ), измеренная ежедневно утром и вечером и записанная пациентом. Бронходилатарующий эффект тиотропия бромида сохранялся в течение всего периода исследования (1 год) без признаков развития толерантности. Рандомизированное плацебо-контролируемое клиническое исследование с участием 105 пациентов с ХОБЛ показало, что бронходилатация сохранялась на протяжении 24-часового интервала дозирования по сравнению с плацебо, независимо от времени введения препарата - утром или вечером.
Клинические исследования (продолжительностью до 12 месяцев)
Одышка, толерантность к физическим нагрузкам
Тиотропия бромид достоверно уменьшал одышку (при оценке с использованием индекса транзиторной одышки). Улучшение сохранялось на протяжении всего периода лечения.
Влияние препарата на выраженность одышки при физической нагрузке была исследована в двух рандомизированных двойных слепых плацебо-контролируемых исследованиях с участием 433 пациентов с умеренной и тяжелой ХОБЛ. В данных исследованиях в течение шестинедельного лечения СПИРИВА продемонстрировано достоверное увеличение времени тренировки на выносливость, ограничиваемое возникновением симптомов, по результатам велоэргометрии, проведенной в режиме 75% от максимальной работоспособности, на 19,7% (исследование А) и 28,3% (исследование В) посравнению с плацебо.
Качество жизни, связанное со здоровьем
В рандомизированном двойном слепом плацебо-контролируемом клиническом исследовании продолжительностью 9 месяцев с участием 492 пациентов лекарственное средство СПИРИВА улучшало общий показатель качества жизни, связанного со здоровьем, оцененный при помощи респираторного опросника Святого Георгия (SGRQ). Количество пациентов, принимавших СПИРИВА и достигших существенного улучшения общего показателя по опроснику SGRQ (т.е. > 4 единиц), было на 10,9% выше, чем в группе плацебо (59,1% в группе СПИРИВА против 48,2% в группе плацебо (р=0,029)). Средняя разница между группами составила 4,19 единицы (р=0,001; доверительный интервал: 1,69-6,68). Улучшение в областях опросника SGRQ составили: 8,19 единицы для области «симптомы», 3,91 единицы для области «деятельность» и 3,61 единицы для области «влияние на ежедневную активность». Улучшение показателей во всех перечисленных областях были статистически значимыми.
Обострение ХОБЛ
В рандомизированном двойном слепом плацебо контролируемом исследовании с участием 1829 пациентов с умеренной до очень тяжелой ХОБЛ тиотропия бромид статистически достоверно уменьшал количество пациентов с обострением ХОБЛ (с 32,2% до 27,8%) и приводил к статистически достоверному уменьшению числа обострений на 19% (от 1,05 до 0,85 случаев/пациент/год воздействия). Госпитализация в связи с обострением ХОБЛ составила 7,0% пациентов в группе тиотропия бромида и 9,5% пациентов в группе плацебо (р=0,056). Количество пациентов, госпитализированных по поводу ХОБЛ, было ниже на 30% (от 0,25 до 0,18 случаев/пациент/год воздействия).
В рандомизированном, двойном слепом исследовании с двойной имитацией, в параллельных группах, продолжительностью 1 год, проводили оценку влияния лечения СПИРИВА 18 мкг один раз в день и салметерола дозированного аэрозоля 50 мкг два раза в день на частоту умеренных и тяжелых обострений с участием 7376 пациентов с ХОБЛ и наличием обострения в течение предыдущего года.
По сравнению с салметеролом СПИРИВА увеличивало время до первого обострения (187 дней по сравнению с 145 днями) с уменьшением на 17% риска развития обострения (отношение рисков 0,83; 95% доверительный интервал (ДИ) 0,77-0,90, р Долгосрочные клинические исследования (более 1 года, до 4 лет)
В рандомизированном двойном слепом плацебо-контролируемом клиническом исследовании продолжительностью 4 года с участием 5993 рандомизированных пациентов (3006 пациентов, получавших плацебо и 2987 пациентов, получавших СПИРИВА) продемонстрировано улучшение ОФВ1 при применении СПИРИВА по сравнению с плацебо, которое сохранялось на протяжении 4 лет. Количество пациентов, завершивших лечение через ≥ 45 месяцев, было выше в группе СПИРИВА по сравнению с группой плацебо (63,8% по сравнению с 55,4%, р
Исследования тиотропия с активным контролем
Долгосрочное крупномасштабное рандомизированное двойное слепое исследование с активным контролем и периодом наблюдения до 3 лет было проведено с целью сравнения эффективности и безопасности СПИРИВА с ингалятором ХандиХалер и СПИРИВА с ингалятором РЕСПИМАТ (5694 пациентов, получавших СПИРИВА ХандиХалер; 5711 пациентов, получавших СПИРИВА РЕСПИМАТ). Первичными конечными точками были время до первого обострения ХОБЛ, время до наступления смертности от любых причин и, в субисследовании (906 пациентов), минимального ОФВ1 (перед введением дозы).
Время до наступления первого обострения ХОБЛ в ходе исследования было численно сопоставимо в группах СПИРИВА ХандиХалер и СПИРИВА РЕСПИМАТ (отношение рисков (СПИРИВА ХандиХалер/СПИРИВА РЕСПИМАТ) 1,02; 95% ДИ 0,97-1,08). Среднее количество дней до первого обострения ХОБЛ составило 719 дней для СПИРИВА ХандиХалер и 756 дней для СПИРИВА РЕСПИМАТ.
Бронхолитическое действие СПИРИВА ХандиХалер продолжалось более 120 недель, и было сходным с действием СПИРИВА РЕСПИМАТ. Средняя разница в минимальном ОФВ! для СПИРИВА ХандиХалер по сравнению со СПИРИВА составила 0,010 л (95% ДИ -0,018-0,038 л).
В постмаркетинговом сравнительном исследовании TIOSPIR между СПИРИВА РЕСПИМАТ и СПИРИВА ХандиХалер продемонстрированы сходные показатели смертности от любых причин, включая отслеживаемые жизненно важные состояния, между исследуемыми группами (отношение рисков (СПИРИВА ХандиХалер/СПИРИВА РЕСПИМАТ) 1,04 с 95% ДИ 0,91-1,19).
Фармакокинетика
Тиотропия бромид является нехиральным четвертичным аммониевым соединением, плохо растворимым в воде. Тиотропия бромид применяется в виде сухого порошка для ингаляций. Обычно при ингаляционном пути введения большая часть вводимой дозы оседает в желудочно-кишечном тракте и, в меньшей степени, достигает легких. Многие данные по фармакокинетике, описанные ниже, были получены при использовании более высоких доз, чем рекомендуемые для лечения.
Абсорбция
После ингаляции порошка у молодых здоровых добровольцев абсолютная биодоступность 19,5% свидетельствует о высокой биодоступости доли препарата, достигающей легких. Растворы тиотропия бромида для приема внутрь имеют абсолютную биодоступность 2-3%.
Максимальные концентрации тиотропия в плазме крови наблюдаются через 5-7 минут после ингаляции. В равновесном состоянии пиковые уровни тиотропия в плазме у пациентов с ХОБЛ составляли 12,9 пг/мл с быстрым снижением в соответствие с многокамерной моделью. Равновесная остаточная плазменная концентрация составила 1,71 пг/мл.
Системное воздействие после ингаляции тиотропия через ингалятор ХандиХалер было сходным с воздействием после ингаляционного введения через ингалятор РЕСПИМАТ.
Распределение
Тиотропий связывается с белками плазмы крови на 72%, объем распределения составляет 32 л/кг. Локальная концентрация в легких не известна, но путь введения предполагает существенно более высокие концентрации препарата в легких. Исследования на крысах показали, что тиотропия бромид не проникает через гематоэнцефалический барьер даже в минимальных количествах.
Биотрансформация
Степень биотрансформации незначительна. Это подтверждается тем, что после внутривенного введения препарата молодым здоровым добровольцам в моче обнаруживается 74% тиотропия бромида в неизмененном виде. Тиотропия бромид - эфир, который неферментативно распадается до спирта (N-метилскопин) и дитиэнилгликолевой кислоты, которые не связываются с мускариновыми рецепторами. В исследованиях in vitro микросомах печени человека и на культуре клеток гепатоцитов человека показано, что некоторая часть препарата (
Выведение
Эффективный период полувыведения тиотропия составляет 27-45 часов у пациентов с ХОБЛ. Общий клиренс после внутривенного введения препарата молодым здоровым добровольцам составлял 880 мл/мин. Внутривенно введенный тиотропия бромид выводится, в основном, почками в неизмененном виде (74%). После ингаляции сухого порошка у пациентов с ХОБЛ почечная экскреция в стационарном состоянии составляет 7% (1,3 мкг) в неизмененном виде в течение 24 часов, оставшаяся неабсорбировавшаяся часть выводится через кишечник. Почечный клиренс тиотропия бромида превышает клиренс креатинина, что подтверждает выведение препарата с мочой. При регулярном ингаляционном применении тиотропия один раз в день у пациентов с ХОБЛ фармакокинетическое стационарное состояние достигалось на 7-й день без признаков кумуляции в последующий период.
Линейность/нелинейность фармакокинетики
Тиотропий демонстрирует линейную фармакокинетику в терапевтических дозах независимо от лекарственной формы.
Особые группы пациентов
Пожилые пациенты
Как и для всех других лекарственных средств с преимущественно почечной экскрецией препарата увеличение возраста пациента ассоциировалось со снижением почечного клиренса тиотропия (с 365 мл/мин. у пациентов с ХОБЛ в возрасте
Нарушения функции почек
При достижении равновесного состояния при ингаляционном введении тиотропия один раз в день у пациентов с ХОБЛ и почечной недостаточностью легкой степени (КК 50-80 мл/мин.) наблюдалось незначительное увеличение AUC0-6,ss (выше на 1,8-30%) и сходные значения Cmax,ss по сравнению с пациентами с нормальной функцией почек (КК > 80 мл/мин.).
У пациентов с ХОБЛ и умеренными или выраженными нарушениями функции почек (КК
Нарушения функции печени
Предполагается, что печеночная недостаточность не оказывает значительного влияния на фармакокинетику тиотропия. Тиотропий выводится преимущественно почками (74% у здоровых молодых добровольцев) и метаболизируется простым неферментативным расщеплением эфира до фармакологически неактивных метаболитов.
Фармакокинетические/фармакодинамические взаимоотношения
Прямая зависимость между фармакокинетикой и фармакодинамикой отсутствует.
Показания к применению
Лекарственное средство СПИРИВА показано в качестве поддерживающей бронходилатирующей терапии с целью облегчения симптомов у пациентов с хронической обструктивной болезнью легких (ХОБЛ).
Способ применения и дозы
Лекарственное средство предназначено только для ингаляционного применения.
СПИРИВА капсулы предназначены только для ингаляций, но не для перорального приема.
Нельзя проглатывать СПИРИВА капсулы.
Следует использовать СПИРИВА капсулы только с ингалятором ХандиХалер.
Особые группы пациентов
Пожилые пациенты могут принимать тиотропия бромид в рекомендуемой дозе.
Пациенты с нарушением функции почек могут использовать тиотропия бромид в рекомендуемой дозе. Информацию об использовании препарата у пациентов с умеренным или выраженным нарушением функции почек (клиренс креатинина ≤ 50 мл/мин.) см. в разделах «Фармакокинетика» и «Меры предосторожности».
Пациенты с нарушением функции печени могут принимать тиотропия бромид в рекомендуемых дозах (см. раздел «Фармакокинетика»).
Дети
ХОБЛ
Опыт применения СПИРИВА у детей и подростков в возрасте до 18 лет по показанию, указанному в разделе «Показания к применению», отсутствует.
Муковисцидоз
Безопасность и эффективность СПИРИВА 18 мкг у детей и подростков не установлены. Данные отсутствуют.
Инструкция по применению ингалятора ХандиХалер
С целью правильного применения лекарственного средства медицинский работник должен показать пациенту, как использовать ингалятор.
Помните, что при использовании лекарственного средства СПИРИВА необходимо тщательно следовать всем указаниям врача.
Ингалятор ХандиХалер специально разработан для СПИРИВЫ. Он не должен использоваться для других лекарственных средств. Вы можете использовать Ваш ХандиХалер в течение одного года.
Ингалятор ХандиХалер включает в себя:
Пылезащитный колпачок; Мундштук; Основание; Прокалывающую кнопку; Центральную камеру. Откройте пылезащитный колпачок, нажав на прокалывающую кнопку до упора, затем отпустите ее. Полностью откройте пылезащитный колпачок, откинув его вверх. Затем откройте мундштук, подняв его вверх. Достаньте капсулу СПИРИВЫ из блистера (непосредственно перед использованием) и поместите ее в центральную камеру (5), как показано на рисунке. Не имеет значения, какой стороной капсула помещается в камеру. Плотно закройте мундштук до щелчка. Оставьте пылезащитный колпачок открытым. Держа ХандиХалер мундштуком вверх, нажмите прокалывающую кнопку один раз до упора, а затем отпустите. Таким образом получается отверстие, через которое препарат высвобождается из капсулы во время вдоха. Полностью выдохните.
Внимание: никогда не выдыхайте в мундштук.
Возьмите ХандиХалер в рот и плотно сожмите губы вокруг мундштука. Держа голову прямо, вдыхайте медленно и глубоко, но в тоже время с достаточной силой, чтобы услышать или почувствовать вибрацию капсулы. Делайте вдох до полного заполнения легких; затем задержите дыхание до ощущения дискомфорта, одновременно вынимая ХандиХалер изо рта. Продолжайте дышать спокойно. Повторите процедуры 6 и 7 до полного опустошения капсулы. Снова откройте мундштук. Выбросьте использованную капсулу. Закройте мундштук и пылезащитный колпачок.
Очистка ХандиХалера
Очищайте Ваш ХандиХалер один раз в месяц. Откройте мундштук и пылезащитный колпачок. Затем, подняв прокалывающую кнопку, откройте основание ингалятора. Тщательно промойте ингалятор теплой водой до полного удаления порошка. Протрите ХандиХалер бумажным полотенцем и с открытыми мундштуком, основанием и пылезащитным колпачком сушите на воздухе в течение 24 часов. После очистки прибора согласно инструкции, он будет готов к следующему использованию. При необходимости наружную поверхность мундштука протрите с помощью влажной, но не мокрой ткани.
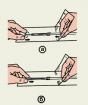
Вскрытие блистера
Отделите полоску блистера по перфорированной линии.Б. Непосредственно перед использованием вскройте полоску блистера таким образом, чтобы одна капсула была полностью видна.
Если капсула была вскрыта случайно и подверглась воздействию воздуха, ее следует выбросить.
Извлеките капсулу.
СПИРИВА капсулы содержат небольшое количество порошка, поэтому капсула заполнена не полностью.
Побочное действие
Многие из нижеперечисленных побочных действий можно отнести к антихолинергическим свойствам СПИРИВЫ.
Частота, указанная для нижеперечисленных нежелательных эффектов, основана на общем уровне встречаемости нежелательного эффекта (т.е. события, связанного с применением тиотропия), наблюдавшихся в группе тиотропия (9647 пациентов) в 28 объединенных плацебо-контролируемых клинических исследованиях с продолжительностью лечения от четырех недель до четырех лет.
Частота определяется следующим образом: очень часто (≥ 1 /10), часто (≥ 1/100 до
Со стороны обмена веществ: неизвестно - дегидратация.
Со стороны нервной системы: нечасто - головокружение, головная боль, нарушения вкуса; редко - бессонница.
Со стороны органа зрения: нечасто - нечеткое зрение; редко - глаукома, повышенное внутриглазное давление.
Со стороны сердца: нечасто - фибрилляция предсердий; редко - наджелудочковая тахикардия, тахикардия, ощущение сердцебиения.
Со стороны дыхательной системы: нечасто - фарингит, дисфония, кашель; редко - бронхоспазм, носовое кровотечение, ларингит, синусит.
Со стороны желудочно-кишечного тракта: часто - сухость во рту; нечасто - гастроэзофагеальный рефлюкс, запор, кандидоз полости рта; редко - кишечная непроходимость, включая паралитический илеус, гингивит, глоссит, затрудненное глотание, стоматит, тошнота; неизвестно - кариес.
Со стороны кожи и подкожных тканей: нечасто - сыпь; редко - крапивница, зуд, гиперчувствительность, включая реакции немедленного типа, ангионевротический отек; неизвестно - анафилактическая реакция, кожные инфекции и язвы, сухость кожи.
Со стороны мышечно-скелетной и соединительной ткани: неизвестно - припухлость суставов.
Со стороны почек и мочевыводящих путей: нечасто - дизурия, задержка мочи; редко - инфекция мочевыводящих путей.
В контролируемых клинических исследованиях наиболее часто встречающиеся нежелательные эффекты были связаны с антихолинергическими свойствами лекарственного средства и проявлялись как сухость во рту у приблизительно 4% пациентов. В 28 клинических исследованиях сухость во рту привела к отмене лечения у 18 из 9647 пациентов, принимавших тиотропий (0,2%).
Серьезные нежелательные эффекты, связанные с антихолинергическими свойствами препарата, включают: глаукому, запор, кишечную непроходимость, включая паралитический илеус, а также задержку мочи.
Частота встречаемости антихолинергических эффектов может увеличиваться с повышением возраста.
Ингалируемые лекарственные средства могут вызвать бронхоспазм.
Тиотропий должен применяться с осторожностью у пациентов с недавним инфарктом миокарда (
В связи с увеличением концентрации препарата в плазме крови у пациентов с умеренным или выраженным нарушением функции почек (клиренс креатинина ≤ 50 мл/мин.), тиотропия бромид может использоваться у данной группы пациентов только в случаях, если предполагаемая польза превышает возможный риск. Данные о длительном применении препарата у пациентов с тяжелой почечной недостаточностью отсутствуют.
Пациентов следует предупредить о том, чтобы они не допускали попадания порошка в глаза. Пациенты должны быть проинструктированы о том, что это может привести к появлению осадка или обострению закрытоугольной глаукомы, боли или чувству дискомфорта в глазах, временному нечеткому зрению, появлению зрительных ореолов или цветных образов в сочетании с покраснением глаз в результате конъюнктивальной гиперемии и отека роговицы. При появлении какого-либо из вышеперечисленных симптомов, пациент должен прекратить прием тиотропия бромида и немедленно обратиться к врачу.
Сухость во рту, наблюдаемая при применении антихолинергических средств, при длительном наличии может привести к появлению кариеса.
СПИРИВА капсулы не следует применять более одного раза в сутки.
СПИРИВА капсулы содержит 5,5 мг лактозы моногидрата. Данное количество обычно не вызывает проблем у пациентов с непереносимостью лактозы. Пациентам с редкими наследственными проблемами непереносимости галактозы, дефицитом лактазы или синдромом мальабсорбции глюкозы-галактозы прием данного лекарства не рекомендуется. Вспомогательное вещество лактозы моногидрат может содержать небольшое количество белков молока, которые могут вызывать аллергические реакции.
Беременность и лактация
Беременность
Данные об использовании тиотропия при беременности очень ограничены. Исследования на животных не выявили прямого или опосредованного неблагоприятного влияния в отношении репродуктивной системы при использовании терапевтических доз. В качестве меры предосторожности предпочтительно избегать применения СПИРИВЫ при беременности.
Период грудного вскармливания
Неизвестно, проникает ли тиотропия бромид в грудное молоко у женщин. Несмотря на то, что в исследованиях на грызунах продемонстрировано, что лишь небольшое количество тиотропия бромида выделяется с грудным молоком, применение СПИРИВА в период грудного вскармливания не рекомендуется. Тиотропия бромид является длительно действующим средством. Решение о необходимости продолжать/прекращать грудное вскармливание или продолжать/прекращать терапию препаратом СПИРИВА следует принимать после оценки преимущества грудного вскармливания для ребенка и пользы терапии СПИРИВА для женщины.
Фертильность
Клинические данные о влиянии тиотропия на фертильность отсутствуют. Доклинические исследования не продемонстрировали отрицательного влияния препарата на фертильность.
Влияние на способность управлять автомобилем и механизмами
Исследования о влиянии тиотропия на способность управлять транспортом и работать с механизмами не проводились. Однако появление головокружения, нечеткости зрения или головной боли при приеме лекарственного средства могут повлиять на способность управления транспортом и работу с механизмами.
Передозировка
При применении тиотропия бромида в высоких дозах возможны проявления антихолинергического действия.
Однако при ингаляционном введении однократной дозы до 340 мкг тиотропия бромида здоровым добровольцам о системных антихолинергических побочных действиях не сообщалось. Кроме того, после 7 дней введения доз тиотропия бромида до 170 мкг здоровым добровольцам не наблюдались побочные эффекты, за исключением сухости во рту. В исследовании с многократными дозами с участием пациентов с ХОБЛ и максимальной суточной дозой тиотропия бромида 43 мкг в течение четырех недель существенных побочных действий не наблюдалось.
Развитие острой интоксикации при случайном приеме внутрь тиотропия бромида капсул маловероятно вследствие низкой биодоступности при пероральном введении.
лекарственными средствами" type="checkbox">
Взаимодействие с другими лекарственными средствами
Хотя специальные исследования взаимодействия с другими лекарственными средствами не проводились, тиотропия бромид порошок для ингаляций применялся в комбинации с другими препаратами, без клинических признаков лекарственного взаимодействия. Указанные препараты включали в себя бронходилататоры (симпатомиметики), метилксантины, пероральные и ингаляционные стероиды, которые широко применяются в лечении ХОБЛ.
Не обнаружено влияния длительно действующих агонистов бета-адренорецепторов или ингаляционных кортикостероидов на экспозицию тиотропия.
Не использовать по истечении срока годности, указанного на упаковке. После вскрытия блистер использовать в течение 9 дней.
Условия отпуска из аптек
По рецепту врача.
Производитель
Берингер Ингельхайм Фарма ГмбХ и Ко. КГ, Германия.
Агентство в РБ
г. Минск, ул. В. Хоружей, 22-1402.
Тел.: (+375 17) 283 16 33, факс: (+375 17) 283 16 40.
Фармакологические свойства
Фармакодинамика. Тиотропия бромид - специфическое антихолинергическое средство с продолжительным действием, обладающим сродством к М1-М5-подтипам мускариновых рецепторов. Конкурентно и обратимо блокируя рецепторы подтипа М3 в дыхательных путях, приводит к расслаблению гладких мышц бронхов. В исследованиях in vitro и in vivo бронходилатирующий эффект был дозозависимым и длился более 24 ч. Такая продолжительность эффекта, вероятно, обусловлена очень медленным высвобождением препарата из связи с М3-рецепторами, что определяет продолжительный период полувыведения и значительно превосходит таковой ипратропия бромида. Являясь четвертичным аммониевым соединением, тиотропия бромид оказывает преимущественно местное действие при ингаляционном применении, его системные антихолинергические эффекты слабо выражены. Диссоциация из связи с M2-рецепторами более быстрая, чем из связи с рецепторами M3 in vitro. М3 - более приемлемый (кинетически контролируемый) подтип рецептора. Высокая эффективность препарата и медленная диссоциация из связи с рецепторами клинически коррелировали со значительно выраженной и продолжительной бронходилатацией у пациентов с ХОБЛ. Бронходилатация после ингаляции тиотропия в первую очередь является местным эффектом на дыхательные пути, а не системным. Применение препарата Спирива 1 раз в сутки сопровождалось значительным повышением функции легких (увеличение объема форсированного выдоха за первую секунду и форсированной жизненной емкости легких) на протяжении 30 мин после ингаляции, продолжительность эффекта составляла 24 ч. Стабильный фармакотерапевтический эффект достигается в течение 1 нед от начала лечения. При ежедневном применении препарат Спирива значительно повышает утреннюю и вечернюю максимальную скорость выдоха. Улучшение функции легких при лечении сохраняется длительный период, признаков развития толерантности к препарату не отмечено. Бронходилатация длится на протяжении 24-часового интервала дозирования по сравнению с плацебо. При этом не учитывался режим приема препарата (утром или вечером). В длительных исследованиях (на протяжении года) установлено: препарат Спирива значительно уменьшает одышку; улучшение состояния удерживалось на протяжении всего периода лечения; значительно уменьшает количество обострений ХОБЛ и прекращает возникновение первого обострения; значительно повышает качество жизни; улучшение отмечалось на протяжении всего периода лечения; значительно сокращает количество госпитализированных пациентов с обострением ХОБЛ, при этом первая госпитализация требуется позже. В 2 исследованиях установлено, что вследствие приема препарата Спирива значительно повысилась толерантность к физической нагрузке, ограниченной симптомами заболевания - на 19,7 и 28,3% соответственно. В исследовании применения 18 и 54 мкг (3 раза в сутки по 18 мкг) Спиривы на протяжении 12 дней не отмечено удлинения интервала Q–T по показателям ЭКГ. Фармакокинетика. Тиотропия бромид является четвертичным аммониевым соединением, которое плохо растворяется в воде, поэтому для ингаляций применяется в виде порошка. Как правило, большая часть дозы, вдыхаемой при ингаляции, оседает на стенках глотки и затем проглатывается, меньшая - оседает на стенках бронхов. После ингаляции сухого порошка у здоровых добровольцев молодого возраста абсолютная биодоступность составляла 19,5%, что является признаком высокой биодоступности фракции, достигающей легких. С учетом химической структуры активного вещества (четвертичное аммониевое соединение) предполагается, что тиотропия бромид лишь в незначительной степени абсорбируется в пищеварительном тракте. По этой же причине одновременный прием пищи не влияет на его абсорбцию. Абсолютная биодоступность тиотропия бромида в виде р-ра для перорального применения составляет 2–3%. Максимальная концентрация тиотропия бромида в плазме крови отмечается через 5 мин после ингаляции. 72% препарата связывается с белками плазмы крови. Объем распределения - 32 л/кг. При равновесном состоянии максимальный уровень тиотропия бромида в плазме крови у пациентов с ХОБЛ составил 17–19 пг/мл при определении через 5 мин после ингаляции в дозе 18 мкг и затем быстро ступенчато снижался. Локальная концентрация в легких не известна, но, исходя из способа применения, допускается высокая концентрация в легких. Тиотропия бромид не проникает через ГЭБ в значительном объеме. Степень биотрансформации незначительная. Тиотропий как сложный эфир неферментативно распадается с образованием спиртового N-метилскопина и дитиэнилгликолевой кислоты, которые не обладают сродством к мускариновым рецепторам. Тиотропий даже в концентрации выше терапевтической не ингибирует цитохром Р450 1А1, 1А2, 2В6, 2С9, 2С19, 2D6, 2Е1 и 3А. Конечный элиминационный период полураспада происходит на 5–6-й день после ингаляции. После ингаляции в виде порошка с мочой выводится 14% дозы, остальное количество не абсорбируется в кишечнике и выводится с калом. Почечный клиренс тиотропия бромида превышает клиренс креатинина, что указывает на выведение с мочой. После постоянной ежедневной ингаляции у пациентов с ХОБЛ равновесное состояние достигается через 2–3 нед без последующей кумуляции. Тиотропий продемонстрировал линейные фармакокинетические свойства в терапевтическом диапазоне после ингаляции сухого порошка. Фармакокинетика у пациентов пожилого возраста Как и для всех других лекарственных средств, которые в основном выводятся с мочой, применение тиотропия у пациентов пожилого возраста связано со снижением почечного клиренса вследствие снижения почечной функции (326 мл/мин у пациентов с ХОБЛ старше 58 лет по сравнению с 163 мл/мин у пациентов с ХОБЛ в возрасте старше 70 лет). Выделение тиотропия в мочу после ингаляции уменьшается с 14% (у здоровых добровольцев молодого возраста) до 7% (у пациентов с ХОБЛ пожилого возраста), однако концентрация в плазме крови существенным образом не изменяется у пациентов с ХОБЛ пожилого возраста и не превышает пределы межиндивидуальной и индивидуальной вариабельности (43% увеличение AUC после ингаляции сухого порошка). Фармакокинетика у пациентов с нарушением функции почек У пациентов с почечной недостаточностью концентрация препарата в плазме крови повышается, а почечный клиренс снижается. При незначительно выраженной почечной недостаточности (клиренс креатинина 50–80 мл/мин) концентрация тиотропия бромида в плазме крови повышается незначительно (увеличение значения AUC после в/в инфузии на 39%). Фармакокинетика у пациентов с нарушением функции печени Печеночная недостаточность не оказывает существенного влияния на фармакокинетику препарата. Тиотропий большей частью выделяется путем почечной элиминации (до 74% у здоровых добровольцев молодого возраста) и путем простого неферментативного расщепления эфира до продуктов, которые не связываются с мускариновыми рецепторами.Показания
поддерживающая терапия у пациентов с ХОБЛ (хронический бронхит и эмфизема легких); поддерживающая терапия одышки, обусловленной ХОБЛ, и профилактика обострений заболевания.Применение
рекомендуемая доза Спиривы - 1 ингаляция (содержимое 1 капсулы) в сутки с помощью ингаляционного устройства ХендиХейлера, проводимая в одно и то же время суток. Капсулы Спиривы не предназначены для приема внутрь. Коррекции дозы препарата у лиц пожилого возраста, пациентов с почечной недостаточностью не требуется, однако больные с умеренно выраженной или тяжелой почечной недостаточностью в период лечения препаратом должны находиться под врачебным наблюдением. Опыт применения Спиривы у детей отсутствует. Устройство ХендиХейлер разработано специально для ингаляций Спиривы, его не следует использовать с другими препаратами. ХендиХейлер можно применять в течение 1 года. Для подготовки устройства к работе следует открыть пылезащитный колпачок, подняв его вверх, затем открыть мундштук. Изъять капсулу Спиривы из блистерной упаковки непосредственно перед применением и разместить ее в центре мембраны устройства (не имеет значения, какой стороной поместить капсулу в камеру). Затем плотно закрыть мундштук (до щелчка), оставив пылезащитный колпачок открытым. Во время ингаляции ХендиХейлер держат мундштуком вверх, нажимают кнопку до упора 1 раз и отпускают, после чего плотно обхватывают губами мундштук и производят вдох. Нельзя выдыхать воздух в устройство. Затем следует повторить вдох из устройства для полного опорожнения капсулы, после чего открыть мундштук снова и вынуть использованную капсулу. Закрыть мундштук и пылезащитный колпачок. Устройство ХендиХейлер следует 1 раз в месяц промывать теплой водой для удаления остатков порошка, после чего тщательно высушить, промокая остаток воды бумажной салфеткой, и просушить на воздухе в течение 24 ч, оставив при этом пылезащитный колпачок, мундштук и основание открытыми. При необходимости мундштук можно очистить с помощью влажной, но не мокрой ткани.Противопоказания
повышенная чувствительность к препарату, атропину или его производным (например к ипратропию или окситропию бромиду) или другим компонентам препарата.Побочные эфекты
многие из перечисленных побочных эффектов можно отнести к антихолинергическим свойствам препарата Спирива. Частота проявлений, приведенная ниже, базируется на данных частоты побочных реакций, которые отмечали у 5437 пациентов, применявших тиотропий, в 19 клинических плацебо-контролируемых исследованиях с периодами лечения от 4 нед до 1 года. Со стороны ЦНС (≥0,1%, но ≤1%): головокружение. Со стороны органа зрения (≥0,01%, но ≤0,1%): нечеткость зрения, повышение внутриглазного давления; глаукома*. Со стороны сердечно-сосудистой системы (≥0,01%, но ≤0,1%): тахикардия, ощущение сердцебиения; суправентрикулярная тахикардия, фибрилляция предсердий*. Респираторные, торакальные и медиастинальные нарушения (≥0,1%, но ≤1%): дисфония, и, как и при применении любых других ингаляционных средств, - бронхоспазм, кашель, раздражение гортани; (≥0,01% и ≤0,1%): носовые кровотечения. Со стороны ЖКТ (≥1%, но ≤10%): сухость во рту, обычно слабо выражена, часто проходит при продолжении лечения; (0,1%, но ≤1%): кандидоз ротовой полости; (≥0,01%, но ≤0,1%): запор, гастроэзофагеальная рефлюксная болезнь; непроходимость кишечника, включающая паралитическую непроходимость, дисфагия. Со стороны иммунной системы, кожи и подкожных тканей (≥0,01%, но ≤0,1%): кожная сыпь, крапивница, зуд и другие аллергические реакции (включая аллергические реакции немедленного типа). Со стороны мочеполовой системы (≥0,01%, но ≤0,1%): нарушение мочеиспускания и задержка мочи (обычно у предрасположенных к этому мужчин), инфекция мочевыводящих путей.Особые указания
Период беременности и кормления грудью. Клинические данные относительно безопасности применения Спиривы в период беременности отсутствуют, однако в экспериментальных исследованиях не выявлено прямого или опосредованного влияния на течение беременности и развитие эмбриона/плода, роды и постнатальное развитие. Клинические данные относительно безопасности применения Спиривы в период кормления грудью отсутствуют, однако экспериментально установлено, что небольшое количество тиотропия бромида проникает в грудное молоко. Препарат не следует применять в период беременности и кормления грудью без тщательной оценки ожидаемой пользы для матери и потенциального риска для плода или ребенка. Исходя из того, что опыт применения Спиривы в лечении детей отсутствует, препарат рекомендуется применять только у взрослых. Спирива является бронходилататором, который назначают 1 раз в сутки для поддерживающей терапии и не применяют для купирования острых приступов бронхоспазма. Как и другие антихолинергические препараты, Спириву необходимо применять с осторожностью у пациентов с закрытоугольной глаукомой, гиперплазией предстательной железы или обструкцией шейки мочевого пузыря. Ингаляционные препараты могут вызвать развитие парадоксального (ингаляционно-индуцированного) бронхоспазма. Пациенты должны быть проинструктированы относительно правильного применения капсул Спиривы. Нельзя допускать попадания порошка в глаза, что может спровоцировать приступ закрытоугольной глаукомы. Признаками закрытоугольной глаукомы могут быть боль или дискомфорт в глазах, нечеткость зрения, появление ореола вокруг предметов или цветных пятен перед глазами в сочетании с гиперемией конъюнктивы или роговицы. Требуется консультация офтальмолога, поскольку применение миотических капель для глаз может быть неэффективно. Спириву не следует использовать более 1 раза в сутки. Капсулы Спиривы следует применять только с устройством ХендиХейлер. Препарат содержит 5,5 мг лактозы моногидрата в одной капсуле. Влияние на способность управлять транспортными средствами и работать с механическими устройствами. Исследования не проводили. Появление головокружения или нечеткости зрения может влиять на способность управлять транспортными средствами и механическими устройствами.Взаимодействие
несмотря на то что формальные исследования взаимодействия с другими лекарственными средствами не проводили, тиотропия бромид применяли одновременно с другими препаратами (симпатомиметические бронходилататоры, метилксантины, пероральные и ингаляционные стероиды, которые применяют в лечении ХОБЛ) без развития побочных эффектов. Недостаточная информация о применении других антихолинергических лекарственных средств сочетанно с препаратом Спирива: одноразовый прием отдельной дозы ипратропия бромида при продолжительном приеме препарата Спирива пациентами с ХОБЛ и здоровыми добровольцами не был связан с увеличением количества побочных реакций, изменением основных показателей состояния организма или результатов ЭКГ. Назначение Спиривы в сочетании с другими лекарственными средствами, содержащими холинолитики, не изучалось и поэтому не рекомендуется.Передозировка
прием препарата Спирива в высоких дозах может вызвать антихолинергические эффекты, хотя в исследовании системные антихолинергические побочные эффекты отсутствовали при назначении препарата здоровым добровольцам в разовой дозе вплоть до 282 мкг. Двусторонний конъюнктивит и сухость во рту отмечали после ингаляции 141 мкг тиотропия в сутки, при продолжении лечения признаки конъюнктивита исчезают. При многократном назначении препарата пациентам с ХОБЛ в суточной дозе 36 мкг на протяжении 4 нед отмечали только ощущение сухости во рту.Условия хранения
при температуре до 25 °С. Не допускать нагревания, замерзания капсул или воздействия на них прямых солнечных лучей. После вскрытия содержимое блистера следует использовать на протяжении 9 дней.Брутто-формула
C 19 H 22 BrNO 4 S 2Фармакологическая группа вещества Тиотропия бромид
Нозологическая классификация (МКБ-10)
Код CAS
139404-48-1Фармакология
Фармакологическое действие - бронхолитическое, м-холиноблокирующее .Фармакодинамика
Тиотропия бромид — м-холиноблокатор продолжительного действия. Обладает одинаковым сродством к различным подтипам мускариновых рецепторов от м 1 до м 5 . Результатом ингибирования м 3 -рецепторов в дыхательных путях является расслабление гладкой мускулатуры. Бронходилатирующий (бронхорасширяющий) эффект сохраняется в течение не менее 24 ч и зависит от дозы тиотропия бромида. Значительная продолжительность действия связана, вероятно, с очень медленной диссоциацией тиотропия бромида от м 3 -рецепторов по сравнению с ипратропия бромидом. При ингаляционном способе введения тиотропия бромид, как N-четвертичное антихолинергическое средство, оказывает местный избирательный эффект, при этом в терапевтических дозах не вызывает системные м-холиноблокирующие нежелательные реакции. Диссоциация тиотропия бромида от м 2 -рецепторов происходит быстрее, чем от м 3 -рецепторов. Высокое сродство к рецепторам и медленная диссоциация обусловливают выраженный и продолжительный бронходилатирующий эффект у пациентов с ХОБЛ . Бронходилатация после ингаляции тиотропия бромида является следствием местного, а не системного эффекта.
Тиотропия бромид значительно увеличивает функцию легких (ОФВ за 1 с — ОФВ 1 , форсированную жизненную емкость легких — ФЖЕЛ) спустя 30 мин после однократной дозы на протяжении 24 ч.
Фармакодинамическое равновесие достигается в течение первой недели, а выраженный бронходилатирующий эффект наблюдается на третий день. Тиотропия бромид значительно увеличивает утреннюю и вечернюю пиковую потоковую скорость выдоха (ПСВ). Применение тиотропия бромида в течение года не вызывает снижение эффективности в отношении бронходилатации.
Тиотропия бромид значительно уменьшает одышку на протяжении всего периода лечения, значительно улучшает переносимость физической нагрузки, существенно снижает число обострений ХОБЛ и увеличивает период до момента первого обострения, а также значительно снижает количество случаев госпитализации, связанных с обострением ХОБЛ , и увеличивает время до момента первой госпитализации. Тиотропия бромид приводит к стойкому улучшению ОФВ 1 после применения в течение четырех лет без изменения темпов ежегодного снижения ОФВ 1 .
Имеются данные о снижении риска смерти на 16% во время лечения тиотропия бромидом, а также данные об увеличении времени до первого обострения со снижением риска развития обострений на 17% при применении тиотропия бромида по сравнению с приемом салметерола.
Также прием тиотропия бромида увеличивает время до наступления первого тяжелого (требующего госпитализации) обострения, снижает ежегодное число средних или тяжелых (требующих госпитализации) обострений.
Фармакокинетика
Всасывание. При ингаляционном способе введения абсолютная биодоступность тиотропия бромида составляет около 19%, что свидетельствует о высокой биодоступности фракции действующего вещества, достигающей легких. C max тиотропия бромида в плазме крови после ингаляции достигается через 5-7 мин. C ss тиотропия бромида в плазме крови у пациентов с ХОБЛ составляет около 12 пг/мл и быстро снижается, что указывает на мультикомпартментный тип распределения тиотропия бромида. В равновесном состоянии базальная концентрация тиотропия бромида в плазме крови составляет около 1,71 пг/мл.
Распределение. Связывание тиотропия бромида с белками плазмы составляет 72% от принятой дозы; V d — 32 л/кг.
Тиотропия бромид не проникает через ГЭБ .
Метаболизм. Степень биотрансформации незначительна. Тиотропия бромид подвергается неферментативному расщеплению по эфирным связям до этанол-N-метилскопина и дитиенилгликолиевой кислоты, которые не связываются с мускариновыми рецепторами. Тиотропия бромид (<20% от дозы после в/в введения) метаболизируется цитохромом P450, этот процесс зависит от оксидации и последующей конъюгации с глутатионом с образованием различных метаболитов. Нарушение метаболизма может иметь место при использовании ингибиторов изоферментов CYP2D6 и CYP3А 4 (хинидин, кетоконазол и гестоден). Таким образом, изоферменты CYP2D6 и CYP3А 4 включаются в метаболизм тиотропия бромида. Тиотропия бромид даже в сверхтерапевтических концентрациях не ингибирует изоферменты CYP1A1 , CYP1А 2, CYP2В 6, CYP2С 9, CYP2С 19, CYP2D6 , CYP2Е 1 или CYP3А в микросомах печени человека.
Выведение. T 1/2 тиотропия бромида после ингаляции варьирует от 27 до 45 ч. Общий клиренс при в/в введении здоровым добровольцам составляет 880 мл/мин. Тиотропия бромид после в/в введения в основном выводится почками в неизмененном виде — 74%. После ингаляции почечная экскреция в равновесном состоянии составляет 7% в сутки от дозы, оставшаяся невсосавшаяся часть выводится через кишечник. Почечный клиренс тиотропия бромида превышает клиренс креатинина, что свидетельствует о его канальцевой секреции. После длительного ингаляционного приема тиотропия бромида однократно в сутки пациентами с ХОБЛ фармакокинетическое равновесие достигается на 7-й день; при этом не наблюдается кумуляция.
Тиотропия бромид имеет линейную фармакокинетику в терапевтических пределах.
Отдельные группы пациентов
Пациенты пожилого и старшего возраста. У пациентов пожилого и старшего возраста наблюдается снижение почечного клиренса тиотропия бромида (365 мл/мин у пациентов с ХОБЛ <65 лет до 271 мл/мин у пациентов с ХОБЛ ≥65 лет). Эти изменения не приводят к соответствующему увеличению значений AUC 0-6 или C max .
Нарушение функции почек. У пациентов с ХОБЛ и легкой степенью почечной недостаточности (Cl креатинина 50-80 мл/мин) ингаляционное применение тиотропия бромида один раз в сутки в равновесном состоянии приводит к повышению значения AUC 0-6 на 1,8-30%. Значение C ss сохраняется таким же, как у пациентов с нормальной функцией почек (Cl креатинина ≥80 мл/мин).
У пациентов с ХОБЛ и средней или тяжелой степенью почечной недостаточности (Cl креатинина <50 мл/мин) в/в применение тиотропия бромида приводит к двукратному увеличению его концентрации в плазме крови (AUC 0-4 увеличивается на 82%, а значение C max — на 52%) по сравнению с пациентами с ХОБЛ и нормальной функцией почек. Аналогичное повышение концентрации тиотропия бромида в плазме крови отмечается и после ингаляции.
Нарушение функции печени. Предполагается, что печеночная недостаточность не оказывает значительное влияние на фармакокинетику тиотропия бромида, т.к. тиотропия бромид в основном выводится почками и с помощью неферментативного расщепления эфирных связей с образованием метаболитов, которые не связываются с мускариновыми рецепторами.
Применение вещества Тиотропия бромид
Поддерживающая терапия у пациентов с ХОБЛ , включая хронический бронхит и эмфизему легких (поддерживающая терапия при сохраняющейся одышке и для предупреждения обострений, улучшения качества жизни, нарушенного вследствие ХОБЛ).
В качестве дополнительной поддерживающей терапии у пациентов с бронхиальной астмой, с сохраняющимися симптомами заболевания на фоне приема по крайней мере ингаляционных ГКС; для уменьшения симптомов бронхиальной астмы, улучшения качества жизни и снижения частоты обострений.
Противопоказания
Повышенная чувствительность к атропину или его производным (в т.ч. ипратропия бромид и окситропия бромид); I триместр беременности; возраст до 18 лет.
Ограничения к применению
Закрытоугольная глаукома, обструкция шейки мочевого пузыря, гиперплазия предстательной железы.
При применении тиотропия бромида следует тщательно наблюдать пациентов со средней и тяжелой степенью почечной недостаточности (Cl креатинина ≤50 мл/мин).
Применение при беременности и кормлении грудью
Данные об использовании тиотропия бромида при беременности у человека ограничены. В исследованиях на животных не получено указаний на прямые или опосредованные неблагоприятные влияния на беременность, развитие эмбриона/плода, процесс родов или постнатальное развитие.
В качестве меры предосторожности предпочтительнее воздержаться от применения тиотропия бромида во время беременности.
Клинических данных о применении тиотропия бромида у женщин, кормящих грудью, не имеется. В доклинических исследованиях были получены данные, что небольшое количество тиотропия бромида экскретируется в грудное молоко.
Тиотропия бромид не должен применяться у беременных или кормящих грудью женщин, если только ожидаемая польза не превышает потенциальный риск для плода или ребенка.
Побочные действия вещества Тиотропия бромид
Нежелательные реакции, представленные ниже, перечислены в соответствии с поражением органов и систем органов и частотой встречаемости. Частота возникновения нежелательных реакций оценивается следующим образом: очень часто — ≥10%; часто — ≥1% и <10%; нечасто — ≥0,1% и <1%; редко — ≥0,01 и <0,1%; очень редко — < 0,01%, включая отдельные сообщения, и частота неизвестна.
Со стороны иммунной системы: редко — крапивница, реакции гиперчувствительности, включая реакции немедленного типа, ангионевротический отек (отек Квинке); частота неизвестна — анафилактические реакции.
Со стороны обмена веществ и питания: частота неизвестна — дегидратация.
Со стороны нервной системы: нечасто — головокружение, головная боль, расстройство вкуса; редко — бессонница.
Со стороны органа зрения: нечасто — нечеткость зрения; редко — повышение ВГД , глаукома.
Со стороны сердца: нечасто — мерцательная аритмия; редко — тахикардия (включая суправентрикулярную тахикардию), ощущение сердцебиения. Со стороны дыхательной системы, органов грудной клетки и средостения: нечасто — дисфония, кашель, фарингит; редко — парадоксальный бронхоспазм, ларингит, синусит, носовое кровотечение.
Со стороны ЖКТ : часто — сухость во рту, обычно легкой степени выраженности; нечасто — запор, гастроэзофагеальный рефлюкс, орофарингеальный кандидоз; редко — тошнота, стоматит, гингвит, глоссит, кишечная непроходимость, включая паралитический илеус, дисфагия; частота неизвестна — кариес.
Со стороны кожи и подкожных тканей: нечасто — сыпь; редко — зуд; частота неизвестна — инфекционные заболевания кожи, язвы на коже, сухость кожи.
Со стороны скелетно-мышечной системы и соединительной ткани: частота неизвестна — припухание суставов.
Со стороны почек и мочевыделительной системы: нечасто — затрудненное мочеиспускание и задержка мочеиспускания (у мужчин с предрасполагающими факторами), дизурия; редко — инфекция мочевыводящих путей.
Взаимодействие
Возможно применение тиотропия бромида в комбинации с другими ЛС , обычно применяющимися для лечения ХОБЛ . Хотя специальных исследований лекарственного взаимодействия не проводилось, тиотропия бромид применялся совместно с симпатомиметиками, метилксантинами, пероральными и ингаляционными ГКС , антигистаминными ЛС , муколитиками, модификаторами лейкотриенов, кромонами, анти-IgЕ ЛС; при этом клинических признаков лекарственного взаимодействия не отмечалось.
Совместное применение с длительно действующими бета 2 -адреномиметиками, ингаляционными ГКС и их комбинациями не влияет на действие тиотропия бромида.
Постоянное совместное применение других антихолинергических ЛС и тиотропия бромида не изучалось и, следовательно, не рекомендуется.
Передозировка
Симптомы: при применении высоких доз тиотропия бромида возможны незначительные проявления системного антихолинергического действия.
Однако системные антихолинергические нежелательные реакции не выявились после однократного ингаляционного применения тиотропия бромида в дозе до 340 мкг здоровыми добровольцами. При применении тиотропия бромида в дозе до 170 мкг здоровыми добровольцами в течение 7 дней не наблюдалось соответствующих нежелательных реакций, за исключением сухости во рту.
Имеются данные, что при применении тиотропия бромида пациентами с ХОБЛ в максимальной суточной дозе 43 мкг более 4 нед не наблюдалось значительных нежелательных реакций.
Острая интоксикация, связанная со случайным приемом капсул внутрь, маловероятна в связи с низкой биодоступностью тиотропия бромида.
Пути введения
Ингаляционно.
Меры предосторожности вещества Тиотропия бромид
Тиотропия бромид как бронходилататор, применяемый один раз в сутки для поддерживающего лечения, не предназначен для начальной терапии при острых приступах бронхоспазма, т.е. в неотложных случаях.
В случае развития острого приступа используются быстродействующие бета 2 -агонисты.
Тиотропия бромид не должен использоваться для лечения бронхиальной астмы в качестве терапии первой линии. Пациентам следует рекомендовать на фоне приема тиотропия бромида продолжать противовоспалительную терапию (например ингаляционные ГКС), даже если симптомы уменьшатся.
После ингаляции тиотропия бромида могут развиваться немедленные реакции гиперчувствительности. Как и другие ингаляционные ЛС , тиотропия бромид может вызывать парадоксальный бронхоспазм.
Пациенты должны быть ознакомлены с инструкцией по применению. Не следует допускать попадания порошка, раствора или аэрозоля тиотропия бромида в глаза. Боль в глазу или дискомфорт, нечеткость зрения, зрительные ореолы в сочетании с покраснением глаз, конъюнктивальным застоем и отеком роговицы могут свидетельствовать об остром приступе закрытоугольной глаукомы. При развитии любой комбинации этих симптомов следует немедленно обратиться к врачу. Применение ЛС , вызывающих миоз, не является эффективным способом лечения в данном случае.
Тиотропия бромид не следует применять чаще чем один раз в день.
Применение тиотропия бромида не влияет на результаты тестов на допинг у спортсменов.
Влияние на способность к управлению автомобилем и другими транспортными средствами, работу с движущимися механизмами. Исследований по изучению влияния тиотропия бромида на способность к вождению автотранспорта и управлению механизмами не проводилось. В случае развития таких нежелательных реакций, как головокружение, головная боль и нечеткость зрения, необходимо воздержаться от вождения автотранспорта и управления механизмами, а также от занятий другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Взаимодействия с другими действующими веществами
Торговые названия
| 0.0007 | |
| 0.0002 |
Холинолитическое, бронходилатирующее средство.
В результате ингибирования М3-рецепторов в дыхательных путях является расслабление гладких мышц бронхов. Высокое сродство к рецепторам и медленная диссоциация от М3- рецепторов обусловливают выраженное и продолжительное бронходилатирующее действие при местном применении у больных с ХОБЛ.
При ингаляционном способе введения абсолютная биодоступность тиотропия бромида составляет 19,5%. В связи с химической структурой (четвертичное аммониевое соединение), тиотропия бромид плохо всасывается из ЖКТ. По этой же причине прием пищи не влияет на абсорбцию тиотропия бромида. Максимальная концентрация в сыворотке крови после ингаляции порошка в дозе 18 мкг достигается через 5 мин и составляет у пациентов с ХОБЛ 17-19 пг/мл, равновесная концентрация в плазме крови —3-4 пг/мл. Связывание с белками плазмы крови 72%, объем распределения — 32 л/кг. Не проникает через ГЭБ. Биотрансформация незначительна, что подтверждается тем, что после в/в введения препарата молодым здоровым добровольцам в моче обнаруживается 74% неизмененного тиотропия. Тиотропий расщепляется неферментативным способом до алкоголь N-метилскопина и дитиенилгликолевой кислоты, которые не связываются с мускариновыми рецепторами. Даже в сверхвысоких дозах тиотропий не игибирует цитохром Р450, 1А1, 1А2, 2В6, 2С9, 2С19, 2D6, 2Е1 или 3А в микросомах печени человека.
После ингаляции терминальный период полувыведения составляет 5-6 дней, выводится почками (14% дозы), остальная часть, неабсорбировавшаяся в кишечнике — с калом.
Бронходилатирующий эффект является следствием местного, а не системного действия, зависит от дозы и сохраняется не менее 24 ч. Применение тиотропия значительно улучшает функцию внешнего дыхания спустя 30 мин после однократной ингаляции на протяжении 24 ч. Равновесное состояние достигалось в течение первой недели, а выраженный бронходилатирующий эффект наблюдался на 3-й день. Оценка бронходилатирующего эффекта на протяжении года не выявила проявления толерантности. Уменьшает количество обострений ХОБЛ, увеличивает период до момента первого обострения по сравнению с плацебо, улучшает качество жизни на протяжении всего периода лечения, уменьшает количество случаев госпитализации, связанной с обострением ХОБЛ и увеличивает время до момента первой госпитализации.
Показания к применению препарата Тиотропия бромид
В качестве поддерживающей терапии у пациентов с ХОБЛ, включая хронический обструктивный бронхит и эмфизему (при сохраняющейся одышке и для предупреждения обострений).
Применение препарата Тиотропия бромид
Ингаляционно с помощью специального ингалятора, по 1 капсуле в сутки в одно и то же время. Капсулы не следует глотать. Люди пожилого возраста, пациенты с нарушенной функцией почек или печени могут применять препарат в рекомендуемых дозах.
Противопоказания к применению препарата Тиотропия бромид
Повышенная чувствительность к тиотропия бромиду, а также к атропину или его производным (например, ипратропию или окситропию), I триместр беременности, возраст до 18 лет.
Побочные эффекты препарата Тиотропия бромид
Со стороны органов ЖКТ —
сухость во рту (обычно легкой степени выраженности, часто исчезает при продолжении лечения), запор.
Со стороны респираторной системы:
кашель, местное раздражение, возможно развитие бронхоспазма, также как и при приеме других ингаляционных средств.
Прочие:
тахикардия, затруднение или задержка мочеиспускания (у мужчин с гиперплазией предстательной железы), ангионевротический отек, нечеткое зрение, острая глаукома (связаны с антихолинергическим действием).
Особые указания по применению препарата Тиотропия бромид
Необходимо тщательное наблюдение за больными с умеренной или тяжелой почечной недостаточностью, получающих тиотропия бромид в комбинации с другими препаратами, экскретирующимися, в основном, почками.
С осторожностью назначают больным с узкоугольной глаукомой, гиперплазией предстательной железы или обструкцией шейки мочевого пузыря.
Нельзя использовать в качестве средства неотложной терапии для купирования приступов бронхоспазма.
Не следует допускать попадания порошка в глаза.
Противопоказано применение в I триместр беременности. В остальные сроки беременности и в период кормления грудью — только в том случае, если ожидаемая польза превышает любой возможный риск для плода или грудного ребенка.
Взаимодействия препарата Тиотропия бромид
Список аптек, где можно купить Тиотропия бромид:
- Санкт-Петербург
При ингаляционном введении тиотропий, как антихолинергическое средство N-четвертичной структуры, оказывает местное избирательное действие, при этом в терапевтических дозах не вызывает системных антихолинергических побочных эффектов. Высвобождение тиотропия из связи с М2-рецепторами происходит быстрее, чем из связи с М3-рецепторами.
Высокое сродство к рецепторам и медленное высвобождение из связи с ними обусловливают интенсивный и продолжительный бронходилатирующий эффект у пациентов с хронической обструктивной болезнью легких (ХОБЛ). Бронходилатация после ингаляции тиотропия является следствием местного, а не системного эффекта.
В клинических исследованиях было показано, что Спирива значительно улучшает функцию легких (объем форсированного выдоха в 1-ю сек /ОФВ1/ и форсированную жизненную емкость легких /ФЖЕЛ/) через 30 мин после однократной дозы на протяжении 24 ч.
Фармакодинамическое равновесие достигалось в течение 1-й недели, а выраженный бронходилатирующий эффект наблюдался на 3-й день. Спирива значительно увеличивает утреннюю и вечернюю пиковую потоковую скорость выдоха, измеряемую больными. Бронходилатирующий эффект Спиривы, оцениваемый на протяжении года, не выявил проявлений толерантности.
Спирива значительно снижает частоту обострений ХОБЛ и увеличивает период до момента первого обострения, по сравнению с плацебо. Значительно улучшает качество жизни, что наблюдается в течение всего периода лечения. Спирива существенно снижает количество случаев госпитализации, связанной с обострением ХОБЛ, и увеличивает время до момента первой госпитализации.
- Фармакокинетика
Тиотропий - четвертичное аммониевое соединение, умеренно растворим в воде. После ингаляции в форме порошка в терапевтическом диапазоне доз характеризуется линейной фармакокинетикой.
При ингаляционном введении абсолютная биодоступность тиотропия составляет 19.5%, что свидетельствует о высокой биодоступности фракции препарата, достигающей легких. C max в плазме крови достигается через 5 мин после ингаляции. Тиотропий плохо всасывается из ЖКТ. По этой же причине прием пищи не влияет на абсорбцию тиотропия.
При приеме внутрь тиотропия в форме раствора абсолютная биодоступность составила 2-3%. Связывание с белками плазмы - 72%. Vd - 32 л/кг. В равновесном состоянии C max в плазме крови у пациентов с ХОБЛ составляет 17-19 пг/мл через 5 мин после ингаляции порошка в дозе 18 мкг и быстро снижается. Css в плазме крови составляли 3-4 пг/мл. Не проникает через ГЭБ.
Степень биотрансформации незначительна. Тиотропий расщепляется неферментным путем до алкоголь-N-метилскопина и дитиенилгликолевой кислоты, которые не связываются с мускариновыми рецепторами. Нарушение метаболизма возможно при применении ингибиторов изоферментов системы цитохрома P450 CYP2D6 и 3A4 (хинидина , кетоконазола , гестодена).
Тиотропий даже в сверхтерапевтических концентрациях не ингибирует изоферменты цитохрома P450 1A1, 1A2, 2B6, 2C9, 2C19, 2D6, 2E1 или 3A4 в микросомах печени человека.
После ингаляционного введения терминальный T 1/2 составляет 5-6 дней. После ингаляции порошка почечная экскреция составляет 14%, остальная часть, не всосавшаяся в кишечнике, выводится с калом. Почечный клиренс тиотропия превышает КК , что свидетельствует о канальцевой секреции препарата.
После длительного приема препарата 1 раз/сут у пациентов с ХОБЛ равновесное состояние фармакокинетических параметров достигается через 2-3 недели, при этом в дальнейшем не наблюдается кумуляции. Тиотропий выводится в основном с мочой в неизмененном виде - 74%.
- Фармакокинетика в особых клинических случаях
У пациентов пожилого возраста наблюдается снижение почечного клиренса тиотропия (326 мл/мин у пациентов с ХОБЛ до 58 лет, до 163 мл/мин у пациентов с ХОБЛ старше 70 лет), что обусловлено, по-видимому, снижением функции почек с возрастом. После ингаляции экскреция тиотропия с мочой снижается с 14% (молодые здоровые добровольцы) до 7% (пациенты с ХОБЛ), однако у пациентов пожилого возраста с ХОБЛ не наблюдалось значительных изменений концентрации в плазме крови, если учитывать меж- и внутрииндивидульную вариабельность (после ингаляции порошка увеличение AUC0-4 на 43%).
При нарушении функции почек после ингаляционного применения повышается концентрация препарата в плазме крови и снижается почечный клиренс. При легкой степени снижения функции почек (КК 50-80 мл/мин), часто наблюдаемой у пациентов пожилого возраста, повышение концентрации тиотропия в плазме крови незначительно.
- Со стороны мочевыделительной системы
Затрудненное мочеиспускание и задержка мочеиспускания (у мужчин с предрасполагающими факторами).
- Аллергические реакции
Реакции повышенной чувствительности, включая единичные случаи ангионевротического отека.
- Прочие
Возможны нечеткость зрения, острая глаукома.
Большинство приведенных выше побочных реакций могут быть связаны с антихолинергическим действием Спиривы.
- Фармакокинетика в особых клинических случаях
- Взаимодействие
Возможно назначение Спиривы в комбинации с другими препаратами, обычно применяющимися для лечения ХОБЛ: симпатомиметиками, производными метилксантина, пероральными и ингаляционными кортикостероидами.
- Передозировка
- Симптомы: возможны незначительные проявления системного антихолинергического действия - сухость во рту, нарушения аккомодации, увеличение ЧСС. После ингаляции однократной дозы до 282 мкг у здоровых добровольцев не выявлено системных антихолинергических эффектов. После повторного приема однократной суточной дозы 141 мкг у здоровых добровольцев наблюдались билатеральный конъюнктивит в сочетании с сухостью во рту, которые исчезали при продолжении лечения. При исследовании, в котором изучались эффекты тиотропия при многократном применении у пациентов с ХОБЛ, получавших максимально 36 мкг препарата более 4 недель, сухость во рту была единственным побочным эффектом. Острая интоксикация, связанная со случайным приемом капсул внутрь маловероятна в связи с низкой биодоступностью препарата.
- Лечение: симптоматическое.
- Меры предосторожности
Препарат Спирива не предназначен для купирования острых приступов бронхоспазма. После ингаляции порошка Спиривы возможно развитие аллергических реакций немедленного типа.
С осторожностью назначать пациентам с закрытоугольной глаукомой, гиперплазией предстательной железы или обструкцией шейки мочевого пузыря.
Процесс ингаляции может вызвать бронхоспазм. Пациентам пожилого возраста следует принимать препарат в рекомендуемых дозах.
При нарушениях функции почек пациенты могут применять Спириву в рекомендуемых дозах. Однако при назначении Спиривы в комбинации с другими препаратами, которые выводятся преимущественно почками, необходим контроль состояния больных. Пациентам с умеренной или тяжелой почечной недостаточностью ( клиренс креатинина ≤ 50 мл/мин) необходимо тщательное наблюдение.
Пациенты с печеночной недостаточностью могут принимать препарат в рекомендуемых дозах.
Пациентов следует ознакомить с правилами использования ингалятора.
Не следует допускать попадания порошка в глаза. Боль в глазах или дискомфорт, нечеткость зрения, зрительные ореолы в сочетании с покраснением глаз, конъюнктивальным застоем и отеком роговицы могут свидетельствовать об остром приступе закрытоугольной глаукомы. При развитии любой комбинации этих симптомов пациент должен немедленно обратиться к врачу. Применение только препаратов, вызывающих миоз, не является эффективным способом лечения в данном случае.