Kondroskyddare vid behandling av degenerativa-dystrofiska sjukdomar i leder och ryggrad. Visa fullständig version Chondroprotectors Research
För citat:Lygina E.V., Miroshkin S.V., Yakushin S.S. Kondroskyddare vid behandling av degenerativa-dystrofiska sjukdomar i leder och ryggrad // BC. 2014. Nr 10. S 762
Kondroskyddare är strukturella element (glykosaminoglykaner) i naturlig broskvävnad som är nödvändiga för konstruktion och förnyelse av ledbrosk. De tillhör gruppen av symtomatiska läkemedel med långsam verkan (Symptomatisk långsamverkande läkemedel för osteoartrit - i den engelska nomenklaturen), har en måttlig smärtstillande effekt och förbättrar lederns funktionella parametrar.
Enligt ett antal prospektiva studier kan kondroprotektorer ha en modifierande effekt på degenerativa dystrofiska sjukdomar i leder och ryggrad (osteoartrit (OA), dorsopati). Bland denna grupp läkemedel finns den största evidensbasen för kondroitinsulfat (CS) och glukosamin (GA). Dessa läkemedel används ofta i en reumatolog och neurolog.
CS är en glykosaminoglykan bestående av långa polysackaridkedjor av upprepande föreningar av disackariden N-acetylgalaktosamin och glukuronsyra. När det gäller kemisk struktur är CS en sulfaterad glykosaminoglykan isolerad från brosket hos fåglar och nötkreatur. Det är en viktig komponent i den extracellulära matrisen i många vävnader, inklusive brosk, ben, hud, artärväggar, ligament och senor. I kroppen är den bildad av HA och består av flera fraktioner som skiljer sig åt i molekylvikt. Dess lågmolekylära fraktioner absorberas nästan fullständigt i mag-tarmkanalen. Farmakokinetiska studier har visat att läkemedlets biotillgänglighet vid oral administrering är cirka 13-15%. Den maximala koncentrationen av kolesterol i blodet detekteras 3-4 timmar efter intag och i synovialvätskan - efter 4-5 timmar. Det utsöndras huvudsakligen av njurarna under dagen. Visar en hög tropism för broskvävnad, men en förutsättning för dess effektivitet är dess ansamling i vävnaderna i leden, därför utvecklas den terapeutiska effekten vanligtvis inom 3-5 veckor. från mottagningens början. Efter avbrytande av läkemedlet fortsätter den terapeutiska effekten i ytterligare 2-3 månader. Läkemedlet tolereras väl av patienter, biverkningar observerades hos endast 2% av patienterna och manifesterade sig som gastralgi, förvärring av kronisk kolecystit, allergiska reaktioner och svullnad i benen. Enligt EULAR är kolesterol det säkraste läkemedlet för behandling av OA; dess toxicitetsvärde är 6 på en 100-punktsskala. Kliniska studier har inte avslöjat några signifikanta biverkningar och oönskade interaktioner med andra läkemedel under långvarig användning.
Verkningsmekanismen för kolesterol är komplex, mångfacetterad och täcker nästan alla viktiga aspekter av patogenesen av OA. CS leder till aktivering av kondrocyter och som en konsekvens ökar deras syntes av proteoglykaner med en normal polymerstruktur. Genom att aktivera synoviocyter leder det till ökad syntes av hyaluronsyra med hög molekylvikt. Det undertrycker aktiviteten hos enzymer som förstör brosk - metalloproteinaser (stromelysin, kollagenas, etc.). Undertrycker för tidig död (apoptos) av kondrocyter, biosyntes av IL-1β och andra inflammatoriska mediatorer. Förbättrar mikrocirkulationen i det subkondrala benet och synoviet. Maskerar sekundära antigena determinanter och undertrycker kemotaxi. Dess antiinflammatoriska effekt är också associerad med hämning av aktiviteten hos lysosomala enzymer, superoxidradikaler och uttrycket av proinflammatoriska cytokiner. Det senare stöds av möjligheten att minska dosen icke-steroida antiinflammatoriska läkemedel (NSAID) under behandling med kolesterol. CS minskar processerna för resorption i det subkondrala benet, undertrycker uttrycket av RANKL och aktiverar syntesen av osteoprotegerin. Således orsakar CS undertryckande av katabolisk och stimulering av anabola processer, har en antiinflammatorisk effekt och förändrar processerna för ombyggnad av det subkondrala benet, vilket underbyggar konceptet för den kondromodifierande effekten av läkemedlet.
HA är en amino monosackarid härledd från kitin isolerad från skalet på kräftdjur. Det finns i form av tre salter: glukosaminhydroklorid, glukosaminsulfat och N-acetylglukosamin. HA, som är en monosackarid, är en föregångare till många glykosaminoglykaner såsom heparansulfat, keratansulfat och hyaluronan. HA är en viktig komponent i cellmembranet och cellytan, spelar en roll i bildandet av brosk, ligament, senor, synovialvätska, hud, ben, naglar, hjärtklaffar och blodkärl. Farmakodynamiken för GA är nära den för CS-läkemedlet. GA stimulerar kondrocyter och ökar deras syntes av proteoglykaner (kondroskyddande effekt). Undertrycker produktionen av IL-1β, TNF-α och andra inflammatoriska mediatorer, minskar produktionen av NO, lysosomala enzymer (antiinflammatorisk effekt).
Verkan av GA och CS har studerats i många kliniska studier. För närvarande finns det tillräckligt med bevis för de symtommodifierande och strukturmodifierande effekterna av dessa läkemedel.
McAlindon et al. (2000) genomförde en metaanalys av 15 dubbelblinda, placebokontrollerade studier (6 för GA, 9 för CS), vars resultat indikerade läkemedlets effektivitet (den standardiserade genomsnittliga skillnaden för GA var 0,44 (95% KI 0,24 0,64) och för CS - 0,78 (95% KI 0,60-0,95)).
Omkring samma tid, T.E. Towheed et al. publicerade data från en systematisk granskning av 16 randomiserade kontrollerade studier som jämför GA och placebo (13 studier), GA och NSAID (3 studier). De belyste den signifikanta heterogeniteten av studier när det gäller administreringsväg för GA, klassificering av OA, utvärderade gemensamma grupper och mätning av slutpunkter. Femton studier undersökte HA-sulfat och en HA-hydroklorid. Författarna visade att GA-behandling ger smärtlindring och förbättrad ledfunktion, liknande andra symtomatiska läkemedel (enkla smärtstillande medel, NSAID), och läkemedlets säkerhet skilde sig inte från placebo.
Metaanalys av CS av B.F. Leeb et al., Som inkluderade 7 dubbelblinda, placebokontrollerade kliniska studier (703 patienter) som varade från 56 till 1095 dagar (de flesta studier varade 90 till 180 dagar), bestämde kolesterolets effektivitet för smärtbehandling lika med 0,9 (95%). CI 0,80-1,0) och för ledfunktion - 0,74 (95% KI 0,65-0,85).
G. Bana et al. analyserade resultaten av 7 randomiserade kliniska prövningar av kolesterol i OA i höft- och knäleder. Det var en signifikant minskning av smärtintensiteten i lederna och Leken-indexet.
Den strukturmodifierande effekten av kolesterol har studerats i flera långvariga, dubbelblinda, placebokontrollerade studier på patienter med OA. I en studie utförd av B. Michel et al., Den strukturella slutpunkten (röntgendynamik av förändringar i fogutrymmets bredd) användes som huvudkriterium för att bedöma kolesterolverkan. Det visades att kolesterolbehandling i en dos av 800 mg / dag under 2 år hade en statistiskt signifikant stabiliserande effekt på bredden på ledutrymmet hos patienter med gonartros.
År 2006, vid sessionen för European Anti-Rheumatic League (EULAR) A. Kahan et al. presenterade resultaten av STOPP-studien, i överensstämmelse med resultaten från tidigare arbete. Baserat på analysen av resultaten av behandlingen med kolesterol i 2 år visade 622 patienter med gonartros en avmattning i sjukdomsprogressionen hos patienter som behandlades med kolesterol jämfört med placebogrupper. I en nyligen metaanalys har M. Hochberg et al. (2008) kom till liknande slutsatser.
L.M. Wildi et al. används för att bedöma den strukturella modifierande effekten av kolesterolmagnetisk resonanstomografi (MRI). En ettårig pilot multicenter randomiserad klinisk studie genomfördes, som inkluderade 69 patienter med gonartros och tecken på synovit. Patienter fick kolesterol i en standarddos på 800 mg / dag. Efter 6 månader. i gruppen som tog kolesterol var det en mindre förlust av den totala volymen brosk (p \u003d 0,03), brosk i sidoregionerna (p \u003d 0,015) och i skenbenet (p \u003d 0,002); liknande resultat kvarstod under observationsperioden. Författarna noterade också en mindre grad av förändringar i det subkondrala benet i huvudgruppen jämfört med kontrollgruppen. Skillnaderna nådde statistisk signifikans 1 år efter studiens start och observerades huvudsakligen i ledens laterala delar.
Användningen av kolesterol i 3 år i OA i lederna i händerna hade en skyddande effekt mot uppkomsten av nya erosioner. Dessa data bekräftades av resultaten av studier av G. Rovetta et al. baserat på behandling av patienter med kolesterol i en dos av 800 mg / dag under 2 år.
Experimentet avslöjade synergism i verkan av kolesterol och GA, vilket manifesterades av en signifikant ökning av produktionen av proteoglykaner av kondrocyter med den kombinerade användningen av dessa ämnen i jämförelse med monoterapi med vart och ett av dessa läkemedel. Således, med monoterapi med kolesterol och GA, ökade produktionen av glykosaminoglykaner av kondrocyter med 32% och med kombinerad terapi - med 96,6%. Detta fungerade som ett experimentellt skäl för den kombinerade användningen av kolesterol och HA, kombinerade preparat innehållande båda dessa ämnen föreföll, till exempel läkemedlet Teraflex, etc.
I USA, för att bedöma den symtommodifierande effekten av dessa läkemedel, genomfördes en multicenter, dubbelblind, placebokontrollerad klinisk studie i parallella grupper på en jämförande studie av effektiviteten av kolesterol, GA-hydroklorid, celecoxib, en kombination av kolesterol och GA-hydroklorid mot placebo hos patienter med gonartros (glukosamin / kondroitinartritintervention GAIT), utförd under överinseende av US National Institutes of Health. Studien inkluderade 1583 patienter (män och kvinnor över 40 år) från 16 medicinska centra med gonartros II-III radiologiskt stadium enligt Kellgren-Lawrence och smärtsyndrom som varade minst 6 månader. De primära effektmåtten i studien var 20% minskning av ledvärk på WOMAC-skalan efter sex månaders behandling. Den strukturmodifierande effekten bedömdes efter 24 månader. Resultaten av en studie som utvärderade läkemedlets effekt på sjukdomssymtom indikerar att kombinationen av kolesterol och GA var effektivare för att minska smärtan i undergruppen av OA-patienter med måttlig till svår knäsmärta jämfört med placebo (79,2 och 54,3 %, respektive; p \u003d 0,002). Författarna kunde dock inte visa den strukturella modifierande effekten av alla läkemedel i jämförelse med placebo; endast hos patienter med de initiala stadierna av OA (II radiologiskt stadium) efter 2 års behandling noterades en avmattning i minskningen av ledutrymmet, även om det inte var signifikant. Förmodligen kräver dessa data detaljerad tolkning, eftersom de inte överensstämmer med de tidigare erhållna resultaten om den strukturella modifieringsåtgärden, till exempel CS. Således, med den kombinerade användningen av CS- och HA-sulfat, observeras en additiv effekt och effektiviteten av behandlingen ökar.
En annan 6-månaders öppen klinisk multicenterstudie utvärderade också effekten, toleransen och eftereffekten av Teraflex hos patienter med kliniskt svår gonartros. Patienterna randomiserades i två grupper: patienter i grupp 1 fick Teraflex, 1 tablett 2 gånger om dagen under den första månaden, sedan 1 tablett en gång / dag i ytterligare 2 månader. i kombination med diklofenak i en dos av 75 mg / dag, patienter i den andra gruppen - diklofenak i en daglig dos på 75 mg. I slutet av den tredje månaden. Efter behandling minskade smärtintensiteten i knäleden avsevärt och den förblev på denna nivå fram till slutet av den sjätte månaden. behandling. Kontrollgruppen visade också positiv dynamik för denna indikator, dock i mycket mindre utsträckning jämfört med huvudgruppen. En liknande trend har noterats för WOMAC funktionsindex.
I en studie av F. Richy et al. den symtommodifierande och strukturmodifierande effekten av kombinationen av GA-hydroklorid och kolesterol utvärderades. Den positiva dynamiken i WOMAC-indexet, normaliseringen av fogarnas funktionella kapacitet och avmattningen av förminskningen av fogutrymmet avslöjades.
Bedömningen av effekten av långvarig terapi med Teraflex på röntgenprogression av gonartros gjordes av M.S. Svetlova. Patienterna delades in i två grupper som var jämförbara med avseende på sjukdomens huvudparametrar. Patienter i huvudgruppen (104 patienter) tog Teraflex enligt det allmänt accepterade schemat i 6 månader, sedan ordinerades läkemedlet genom upprepade kurser med 2 kapslar per dag i 2 månader. med ett intervall på 1 månad. Den totala behandlingstiden var 3 år. Patienter i kontrollgruppen (140 patienter) ordinerades diklofenak 100 mg / dag i kombination med olika typer av sjukgymnastik. Alla patienter genomgick röntgen av knälederna i frontala, laterala och axiella utsprång i positionen för maximal knäförlängning. Graden av förträngning av ledutrymmet och svårighetsgraden av osteofytos bedömdes med en halvkvantitativ metod. Röntgenprogression vid slutet av det första behandlingsåret detekterades i 8,6% av fallen i huvudgruppen och hos 9,2% - i kontrollgruppen efter 2 års behandling - i 15,4 respektive 18,3% av fallen och efter 3 år - i 21,4 och 32,7%.
Även M.S. Svetlova genomförde en studie som utvärderade den symtommodifierande effekten av långvarig (under ett år) behandling med Theraflex hos patienter med coxartros (CA). Huvudgruppen inkluderade 44 patienter med CA. Alla patienter i huvudgruppen ordinerades Teraflex traditionellt i 6 månader och sedan - genom upprepade kurser med 2 kapslar per dag i 2 månader. med en paus på 1 månad var läkemedlets totala varaktighet 10 månader. När smärtan i lederna ökade tog patienterna NSAID. Kontrollgruppen bestod av 28 patienter med CA. Patienter i kontrollgruppen rekommenderades att ta NSAID i kombination med olika typer av sjukgymnastik. När en positiv effekt uppnåddes ordinerades NSAID endast när smärtan i lederna ökade. Hos patienter i huvudgruppen efter 6 månader. kontinuerlig användning av Teraflex minskade svårighetsgraden av smärta vid gång och i vila, stelhet, förbättrad funktion hos de drabbade lederna. Det positiva resultatet kvarstod efter ett års intag av läkemedlet upprepade gånger och skilde sig avsevärt från de ursprungliga värdena. Under behandling med Teraflex efter 6 månader. observation av ungefär hälften av patienterna kunde helt sluta ta NSAID eller minska deras dagliga dos signifikant. I kontrollgruppen efter 6 månader. behandlingen visade också en viss positiv dynamik hos kliniska indikatorer, men efter 1 år skilde sig värdena inte signifikant från de ursprungliga.
Enligt EULAR från 2003 är användningen av NSAID och kondroprotektorer vid behandling av OA den mest effektiva (bevisklass IA). Ett antal ryska och utländska forskare har under långvariga prospektiva observationsstudier visat att ledvärk vid OA är en av de oberoende prediktorerna för sjukdomsprogression. Smärtreduktion är huvudmålet för OA-behandling. Den största förekomsten av OA förekommer i gruppen äldre och senila patienter, som ofta har samtidig sjukdomar som kräver läkemedelsbehandling. Intag av NSAID förvärrar förloppet av arteriell hypertoni (AH), minskar effektiviteten av blodtryckssänkande behandling och kan förvärra hjärtsvikt. Utvecklingen av NSAID-gastropati, NSAID-enteropati, NSAID-associerad dyspepsi är välkänd, vars ökning av frekvensen observeras hos äldre. Vid användning av HA och CS observeras en extremt låg frekvens av biverkningar. Med tanke på att metabolismen av dessa läkemedel sker utan deltagande av cytokrom P450-systemet är risken för negativ interaktion med andra läkemedel osannolik. Tillsammans med de symtommodifierande och strukturmodifierande effekterna av GA och CS bestämmer detta delvis deras utbredda användning, särskilt i äldre åldersgrupper bland patienter med hög comorbiditet och åldersrelaterade förändringar i inre organs funktioner. Användningen av kolesterol och GA i OA stöds av den ryska föreningen för reumatologi, utländska reumatologiska föreningar, EULAR och OARSI-rekommendationer.
Under de senaste åren har ett antal forskare rekommenderat användning av CS vid den komplexa behandlingen av vertebrogena sjukdomar i nervsystemet. Enligt ICD-10 är dorsopatier uppdelade i deformerande dorsopatier, spondylopatier och andra dorsopatier (degeneration av intervertebrala skivor, sympatiska syndrom). I de flesta fall orsakas neurologisk patologisk ryggrad av degenerativ-dystrofiska förändringar i ryggraden (förstörelse av intervertebrala skivor, spondyloarthrosis, stenos i ryggraden och intervertebral foramen) och representeras av dorsopatier. Den främsta manifestationen av dorsopati är ryggont.
Det bör noteras att evidensbasen för effektiviteten vid användning av kondroprotektorer i dorsopatier är mer knapp än i OA för stora leder, men det finns ett antal publikationer som ägnas åt detta problem.
För första gången användes CS i ryggradspatologi av K.D. Christensen et al. 1989; I sitt arbete har forskare visat effektiviteten av kolesterol för kronisk smärta i nedre delen av ryggen.
A.V. Chebykin utvärderade effektiviteten av införandet av kondroskyddare i den komplexa behandlingen av patienter med ospecifik ryggsmärta. Patienter i huvudgruppen (1430 personer) fick tillsammans med standardbehandling (NSAID, muskelavslappnande medel, icke-läkemedelsbehandling) en kombination av kolesterol (500 mg) och GA (500 mg) oralt i 6 månader. Kontrollgruppen (118 personer) fick endast standardterapi. I huvudgruppen uppstod en ihållande minskning av smärtsyndrom enligt den visuella analoga skalan (VAS), normalisering av rörelseomfånget i lederna i ryggraden, en minskning av behovet av NSAID och i vissa fall vägran att ta dessa läkemedel, en förbättring av livskvaliteten. Effekten av kondroprotektorer manifesterades pålitligt efter 3-4 månader. behandling ökade med 6 månader. och kvarstod i minst 5 månader. efter avslutad behandling. Hos patienter i kontrollgruppen, med tillbakadragande av NSAID och muskelavslappnande medel, ökade smärtan gradvis. graden av smärtsyndrom efter 1 år var signifikant högre än i huvudgruppen.
Liknande resultat erhölls av andra forskare som använde kondroprotektorer vid behandling av patienter med degenerativ-dystrofiska sjukdomar i ryggraden. T.V. Chernysheva et al. utvärderade den antiinflammatoriska, smärtstillande och kondroskyddande effekten av kolesterol under långvarig behandling av kliniskt signifikant osteokondros (OC) i ländryggen. Läkemedlets effektivitet och tolerabilitet studerades i en öppen kontrollerad studie; patienterna delades in i två grupper (huvud och kontroll), 40 personer vardera. Patienter i huvudgruppen fick 100 mg kolesterol intramuskulärt varannan dag, behandlingsförloppet var 20 injektioner; efterföljande kurser hölls med 6 månaders intervall. inom två år. Patienter i båda grupperna tog NSAID vid behov. Hos patienter i kontrollgruppen var NSAIDs den enda behandlingen för förvärringar av AC i ryggraden. Hos patienter i huvudgruppen, förutom att minska smärtsyndromet och behovet av att ta NSAID, förbättra rörligheten i ländryggen, minska frekvensen och varaktigheten av AC-förvärringar, signifikant (p<0,05) уменьшение фрагментации фиброзного кольца верхних межпозвонковых дисков поясничного отдела (L1-2, L2-3, L3-4) по данным ультразвукового исследования. Случай регенерации межпозвонкового диска у пациента, страдающего болью в спине, ассоциированной с дегенеративной болезнью диска, на фоне 2-летнего приема хондропротекторов описан также W.J. van Blitterswijk и соавт. . Таким образом, доказано не только симптом-модифицирующее, но и структурно-модифицирующее действие ХС при дегенеративно-дистрофической патологии позвоночника.
Effektivitet och tolerans av CS hos patienter med smärta i nedre delen av ryggen orsakad av degenerativ-dystrofiska förändringar i ryggraden och samtidig patologi i det kardiovaskulära systemet (IHD och AH) studerades av V.I. Mazurov et al. ... Kolesterol ordinerades i 6 månader. (under de första 20 dagarna, 1500 mg, sedan 1000 mg). I slutet av den första månaden. betydande behandling (s<0,05) уменьшение интенсивности боли по ВАШ как при движении (на 27%), так и в покое (на 22%). К 6-му мес. наблюдалось достоверное (р<0,01) увеличение подвижности позвоночника по данным функциональных позвоночных проб. При динамической оценке индекса хронической нетрудоспособности Вадделя выявлено значительное повышение переносимости бытовых, социальных и спортивных нагрузок. 27% больных отказались от приема НПВП из-за отсутствия боли через 1 мес. терапии, 32% - через 3 мес., 42% - через 6 мес. Через 3 мес. после отмены ХС сохранялся его достоверный (р<0,01) клинический эффект; через 6 мес. эффект последействия препарата снизился, но показатели болевого синдрома были ниже, чем до лечения. Подавляющее большинство пациентов отметили хорошую переносимость ХС; побочные эффекты (гастралгия, крапивница) наблюдались в единичных случаях. При оценке клинического течения ИБС не было отмечено достоверных различий по частоте возникновения ангинозных болей, аритмий, выраженности хронической сердечной недостаточности с исходными данными в ходе 6-месячной терапии ХС. Через 1 мес. от начала приема ХС на фоне постепенного уменьшения потребности в НПВП констатировано снижение АД у пациентов с АГ, что позволило уменьшить среднесуточную дозу антигипертензивных препаратов. Исследователи полагают, что уменьшение потребности в НПВП при терапии ХС приводит к повышению синтеза вазодилатирующих простагландинов и простациклина, что стабилизирует течение ИБС и АГ.
Med tanke på synergismen i GA och CS, rekommenderar ett antal forskare att förskriva en kombination av dessa läkemedel för dorsopatier. Den optimala synergistiska effekten uppnås när man använder GA och CS i förhållandet 5: 4; det är i denna andel som dessa ämnen ingår i Teraflex-beredningen. Enligt den prognostiska modellen, bör den maximala effekten av Teraflex förväntas i de inledande stadierna av degenerativa-dystrofiska lesioner i ryggraden; kliniskt betyder detta användning av läkemedlet efter det första återfallet av ospecifik ryggsmärta, särskilt i närvaro av symtom på spondyloartros. I det här fallet har kursbehandlingen en profylaktisk effekt på kronisk smärta. Läkemedlet kan dock vara användbart vid en detaljerad bild av spondyloartros; i det här fallet kan man förvänta sig en stabilisering av tillståndet och en avmattning i processen.
Vid förskrivning av kondroskyddande behandling för dorsopati under en smärtsam episod är Teraflex Advance att föredra, eftersom detta läkemedel också innehåller NSAID. Efter smärtlindring är det rationellt att byta till att ta Teraflex. Hos de allra flesta patienter som använder Teraflex finns en positiv trend i form av smärtlindring och en minskning av neurologiska symtom.
De presenterade uppgifterna indikerar att CS och HA inte bara har symtommodifierande utan också strukturmodifierande egenskaper, och de kan betraktas som ett medel för patogenetisk terapi av degenerativ-dystrofiska sjukdomar i leder och ryggrad.
Litteratur
- Jordan K.M. et al. EULAR-rekommendation 2003: ett evidensbaserat tillvägagångssätt för hantering av knäartros: Rapport från en arbetsgrupp från ständiga kommittén för internationella kliniska studier inklusive terapeutiska prövningar (ESCISIT) // Ann. Reum. Dis. 2003. Nr 62. S. 1145-1155.
- Leeb B.F., Schweitzer H., Montag K., Smolen J.S. En metaanalys av kondroitinsulfat vid behandling av artros // J. Rheum. 2000. Nr 27. S. 205-211.
- V.A. Nasonova, E.L. Nasonov Rationell farmakoterapi av reumatiska sjukdomar. Moskva: Litera, 2003.507 s.
- Volpi N. Oral biotillgänglighet av kondroitinsulfat (kondrosulf) och dess beståndsdelar hos friska manliga frivilliga // Osteoartrit brosk. 2002. Vol. 10, nr 10. s. 768-777.
- Hathcoock J.N., Shao A. Riskbedömning för glukosamin och kondroitinsulfat // Regul. Toxicol. Pharmacol. 2007. Vol. 47, nr 1. s. 78-83.
- Alekseeva L.I., Sharapova E.P. Kondroitinsulfat vid behandling av artros // Ros. honung. tidskrift. 2009. Vol. 17, nr 21. S. 1448-1453.
- Monfort J. et al. Kondroitinsulfat och hyaluronsyra inhiberar stromelysin-1-syntes i humana artros kondrocyter // Drugs Exp. Clin. Res. 2005. Vol. 31. s. 71-76.
- Caraglia M. et al. Alternativ behandling av jordelement ökar kondroitinsulfat hos kondroitinsulfat hos möss // Exp. Mol. Med. 2005. Vol.37. S. 476-481.
- Chan P.S., Caron J.P., Orth M.W. Kortvariga förändringar av genuttryck i broskexplantat stimulerade med interleukin beta-glukosamin och kondroitinsulfat // J. Rheumatol. 2006. Vol. 33. s. 1329-1340.
- Holzmann J. et al. Blandade effekter av TGF-beta och kondroitinsulfat på p38 och ERK ½ aktiveringsnivåer i humana ledkondrocyter stimulerade med LPS // Osteoartrit brosk. 2006. Vol.14. S. 519-525.
- Monfort J., Pellietier J.-P., Garcia-Giralt N., Martel-Pellietier J. Biokemisk bas för effekten av kondroitinsulfat på artrosvävnader artros // Ann. Reum. Dis. 2008. Vol. 67. s. 735-740.
- Chichasova N.V., Mendel O.I., Nasonov E.L. Artros som ett allmänt terapeutiskt problem // BC. 2010. Vol. 18, nr 11. S. 729-734.
- V.E. Novikov Chondroprotectors // Recensioner om kilen. odla. och läkemedel. terapi. 2010. T. 8, nr 2. S. 41-47.
- Kwan Tat S. et al. Differentialuttrycket av osteoprotegerin (OPG) och receptorn för kärnfaktor kB-ligand (RANKL) i humana osteoartritiska subkondrala osteoblaster är en indikator på det metaboliska tillståndet hos dessa sjukdomsceller // Clin. Exp. Reum. 2008. Vol. 26. s. 295-304.
- Alekseeva L.I. Långsamverkande symtomatiska läkemedel vid behandling av artros // Consilium Medicum. 2009. V. 11, nr 9. S. 100-104.
- Annefeld M. Nya data om glukosaminsulfat // Vetenskaplig och praktisk reumatologi. 2005. Nr 4. S. 76-80.
- Registrera J. et al. Glukosaminsulfat saktar ner artros progressin hos postmenopausala kvinnor: poolad analys av två stora, oberoende, randomiserade dubbelblinda placebokontrollerade, prospektiva 3-åriga studier // Ann. Reum. Dis. 2002. Vol. 61 (tillägg 1). THU 0196.
- McAlindon T.E., LaValley M.P., Gulin J.P., Felson D.T. Glukosamin och kondroitin för behandling av artros: en systematisk kvalitetsbedömning och metaanalys // JAMA. 2000. Vol. 283. s. 1469-1475.
- Towbeed T.E., Maxwell L., Anastassiades T.P. et al. Glukosaminbehandling för behandling av artros // Cochrane Database Syst. Varv. 2005. Vol. 2.
- Leeb B.F., Schweitzer H., Montag K., Smolen J.S. En metaanalys av kondroitinsulfat vid behandling av artros // Artros Brosk. 1999. Vol. 7 (Suppl A). Abstr. 130.
- Bana G., Jamard B., Verrouil E., Mazieres B. Chondroitinsulfat vid hantering av höft och knä OA: en översikt // Adv. Pharmacol. 2006. Vol. 53. s. 507-522.
- Michel B.A. et al. Kondroitin 4 och 6 sulfateinartros i knäet: En randomiserad, kontrollerad studie // Arthritis Rheum. 2005. Vol. 52. s. 779-786.
- Wildi L.M. et al. Kondroitinsulfat minskar både förlust av broskvolym och benmärgsskador hos knäartrospatienter som börjar så tidigt som 6 månader efter behandlingsstart: en randomiserad, dubbelblind, placebokontrollerad pilotstudie med MR // Ann. Reum. Dis. 2011. Vol. 70 (6). R. 982-989.
- Verbuggen G., Goemaere S., Veys E.M. Kondroitinsulfat: S / DMOAD (struktur / sjukdomsmodifierande läkemedel mot artros) vid behandling av fingerled OA // Artros Brosk. 1998. Vol. 6 (tillägg A.). S. 37-38.
- Rovetta G., Monteforte P., Molfetta G., Balestra G. En tvåårsstudie av kondroitinsulfatein erosiv artros i bandet: beteende av erosioner, osteofyter, smärta och handdysfunktion // Läkemedel. Exp. Clin. Res. 2004. Vol. 30 (1). P.11-16.
- Lippielo L., Grande D. In vitro kondroskydd av glukosamin och kondroitinsulfat i en kaninmodell av en OA och demonstration av metabolisk synergi på kondrocyt in vitro // Ann. Reum. Dis. 2000. Vol. 59 (tillägg 1). S. 266.
- Leela A.M. och andra. Teraflex i den komplexa behandlingen av artros i knälederna och osteokondros i ryggraden // Rosmed. tidskrift. 2005. T. 13, nr 24. S. 1618-1622.
- Clegg D.O. et al. Glukosamin, kondroitinsulfat och de två i kombination för smärtsam knäartros // N. Engl. J. Med. 2006. Vol. 354. S. 795-808.
- Richy F. et al. Strukturell och symptomatisk effekt av glukosamin och kondroitin vid knäartros: En omfattande metaanalys // Arch. Internera. Med. 2003. Vol.163. S. 1514-1522.
- Svetlova M.S. Diagnostik och strukturmodifierande behandling av knäledsartros // Modern reumatologi. 2012. Nr 1. S. 38-44.
- Svetlova M.S. Artros i höftleden: klinisk bild, diagnos, tillvägagångssätt för behandling // Modern reumatologi. 2013. Nr 1. S. 46-50.
- Rachin A.P. Bevisbaserad farmakoanalytik för behandling av artros // Pharmateka. 2007. nr 19. S. 81-86.
- Kashevarova N.G., Zaitseva E.M., Smirnov A.V., Alekseeva L.I. Smärta som en av riskfaktorerna för utvecklingen av artros i knäleden // Vetenskaplig och praktisk reumatologi. 2013. Nr 4. S. 387-390.
- Dieppe P., Cushnaghan J., Young P., Kirwan J. Förutsägelse av utvecklingen av ledutrymmets förträngning vid artros i knäet genom benscintigrafi // Ann. Reum. Dis. 1993. Vol. 52. s. 557-563.
- Cooper C. et al. Riskfaktorer för förekomst och progression av radiografisk knäartros / // Artrit. Reum. 2000. Vol. 43. s. 995-1000.
- Conaghan P.G. et al. Kliniska och ultrasonografiska prediktorer för ledersättning för knäartros: resultat från en stor 3-årig prospektiv EULAR-studie // Ann. Reum. Dis. 2010. Vol. 69. s. 644-647.
- Savenkov M.P., Brodskaya S.A., Ivanov S.N., Sudakova N.I. Inverkan av icke-steroida läkemedel på den antihypertensiva effekten av ACE-hämmare // BC. 2003. Nr 19. S. 1056-1059.
- Heerdink E.R. et al. NSAID associerade med ökad risk för hjärtsjukdom hos äldre patienter som tar diuretika // Arch. Int. Med. 1998. Vol. 158. s. 1108-1112.
- Page J., Henry D. Konsumtion av NSAID och utveckling av hjärtsvikt hos äldre patienter // Arch. Int. Med. 2000. Vol.160. S. 777-784.
- Warksman J.C. Icke-selektiva icke-steroida antiinflammatoriska läkemedel och kardiovaskulär risk: är de säkra? // Ann. Rharmacother. 2007. Vol. 41. R.1163-1173.
- Reumatologi. Kliniska riktlinjer / Ed. E.L. Nasonov. M.: GEOTAR-Media, 2010.752 s.
- Kliniska riktlinjer. Artros. Diagnostik och hantering av patienter med artros i knä och höftleder / Ed. O. M. Lesnyak. Moskva: GEOTAR-Media, 2006.176 s.
- Tugwell P. Philadelphia-panelen bevisbaserade kliniska riktlinjer för utvalda rehabiliteringsåtgärder för knäsmärta // Phys. Ther. 2001. Vol. 81. s. 1675-1700.
- Conaghan P.G., Dickson J., Grant R.L. Vård och hantering av artros hos vuxna: sammanfattning av NICE-vägledning // BMJ. 2008. Vol.336. R. 502-503.
- Nationellt samarbetscenter för kroniska tillstånd. Artros: nationell klinisk riktlinje för vård och hantering hos vuxna. London: Royal College of Physicians, 2008.316 s.
- Zhang W. et al. EULAR evidensbaserade rekommendationer för hantering av höftartros: rapport från en arbetsgrupp från EULARs ständiga kommitté för internationella kliniska studier inklusive terapeutik (ESCISIT) // Ann. Reum. Dis. 2005. Vol. 64. s. 669-681.
- Zhang W. et al. EULAR evidensbaserade rekommendationer för hantering av handartros: rapport från en arbetsgrupp från EULAR: s ständiga kommitté för internationella kliniska studier inklusive terapeutik (ESCISIT) // Ann. Reum. Dis. 2007. Vol. 66. s. 377-388.
- Zhang W. et al. OARSI-rekommendationer för hantering av höft- och knäartros, del II: OARSI evidensbaserade riktlinjer för expertkonsensus // Artrosbrosk. 2008. Vol.16. S. 137-162.
- Zhang W. et al. OARSI-rekommendationer för hantering av höft- och knäartros: del III: Förändringar i bevis efter systematisk kumulativ uppdatering av forskning publicerad till januari 2009 // Artros Brosk. 2010. Vol.18. S. 476-499.
- Alekseev V.V. Kondroskydd i neurologi: skäl för användning // Consilium Medicum. Neurologi. Reumatologi. 2012. Nr 9. S.110-115.
- Alekseev V.V., Alekseev A.V., Goldzon G.D. Ospecifik smärta i nedre delen av ryggen: från symptomatisk behandling till patogenetisk // Zhurn. neurologi och psykiatri dem. S.S. Korsakov. 2014. Nr 2. S. 51-55.
- V.V. Badokin Artra-läkemedel - en modell för kombinerad symtommodifierande behandling av artros och intervertebral osteokondros // Neurologi, neuropsykiatri, psykosomatika. 2012. Nr 2. S. 91-95.
- A. V. Chebykin Erfarenhet av att använda kondroprotektor Arthra hos patienter med ryggsmärta // Neurologi, neuropsykiatri, psykosomatika. 2012. Nr 3. S. 69-71.
- Christensen K.D., Bucci L.R. Jämförelse av näringstillskottets effekter på funktionella bedömningar av nedre ryggpatienter mätt med en objektiv datorassisterad testare // Andra symposiet om näring och kiropraktik. Davenport: Palmer College of Chiropractic, 1989. S. 19-22.
- Shostak N.A. och andra Smärta i nedre delen av ryggen vid osteokondros i ryggraden: erfarenhet av användning av ett kondroskyddande läkemedel // Ter. arkiv. 2003. Nr 8. S. 67-69.
- Cox J.M. Ländryggssmärta: mekanism, diagnos och behandling. Baltimore: Williams & Wilkins, 1999.735 s.
- Gorislavets V.A. Strukturmodifierande terapi av neurologiska manifestationer av osteokondros i ryggraden // Consilium Medicum. 2010. nr 9. S. 62-67.
- PÅ. Shostak et al. Dorsopathies - metoder för diagnos och behandling // Svår patient. 2010. Nr 11. S. 22-25.
- T.V. Chernysheva, G.G. Bagirova Två års erfarenhet av att använda kondrolon för osteokondros i ryggraden // Kazan Med. zhurn. 2009. Nr 3. S. 347-354.
- Van Blitterswijk W.J., van de Nes J.C., Wuisman P.I. Tillägg av glukosamin och kondroitinsulfat för att behandla symtomatisk skivegeneration: biokemisk grund och fallrapport // BMC-komplement Altern Med. 2003. Vol. 3. URL: http://www.biomedcentral.com/1472-6882/3/2 (datum för åtkomst: 03/11/2014).
- Mazurov V.I., Belyaeva I.B. Användningen av struktum vid den komplexa behandlingen av smärtsyndrom i nedre delen av ryggen // Ter. arkiv. 2004. Nr 8. S. 68-71.
- Manvelov L.S., Tyurnikov V.M. Ländryggsmärta (etiologi, klinisk bild, diagnos och behandling) // Ros. honung. zhurn. Neurologi. Psykiatri. 2009. nr 20. S. 1290-1294.
- Vorobieva O.V. Rollen hos ryggraden i bildningen av kroniskt smärtsyndrom. Frågor om terapi och förebyggande // Ros. honung. zhurn. 2010. nr 16. S. 1008-1013.
V.V. KOSAREV, MD, DSc, professor, S.A. BABANOV, MD SBEE HPE "Samara State Medical University" från Rysslands hälsovårdsministerium
EFFEKTIVITET AV MODERNA KONDROBESKYTTARE
I OSTEOARTHROSIS
Nyckelord: artros, ledbrosk, kondrocyter, långsamt verkande symptommodifierande läkemedel, kondroitinsulfat, glukosamin
Artros (OA) är en grupp av gemensamma sjukdomar av olika etiologier som orsakar förstörelse av brosk och gradvis leder till dess förlust.
Artros tar ledande plats bland sjukdomar i muskuloskeletala systemet. Enligt WHO lider mer än 4% av världens befolkning av artros, i 10% av fallen är det orsaken till funktionshinder, vilket försämrar livskvaliteten och den sociala anpassningen hos patienter. Bland personer i åldern 65 år är OA-frekvensen 50%, över 75 år - upp till 80%. Förekomsten av artros i Ryska federationen är 580 per 100 tusen invånare. I strukturen av reumatiska sjukdomar upptar OA upp till 70%. Enligt prognoser kan förekomsten av artros fördubblas på tio år.
För närvarande anses artros vara en kronisk progressiv sjukdom i synovial
leder, som utvecklas som ett resultat av ett komplext komplex av biomekaniska, biokemiska och / eller genetiska faktorer. Kärnan i degenerativa dystrofiska förändringar i OA är den primära skadan på brosk följt av en inflammatorisk reaktion. Den patologiska processen i OA involverar inte bara ledbrosket utan också det subkondrala benet, ledband, ledkapsel, synovium och periartikulära muskler. OA är alltid förknippat med deformation av benvävnaden, och därför kallas det också deformerande artros.
De viktigaste kliniska symptomen på OA är smärta och deformation av lederna, vilket leder till deras funktionsfel. Det finns lokaliserade (med skador på en led) och generaliserade former av artros (polyosteoartrit).
Om orsaken till utvecklingen av sjukdomen inte är fastställd kallas artros primär eller idiopatisk.
OA kan uppstå som ett resultat av interaktionen mellan olika interna (ålder, kvinnligt kön, klimakteriet hos kvinnor, utvecklingsdefekter, ärftlig predisposition) och yttre faktorer (trauma, överdriven stress), vilket leder till skada på ledbrosket och / eller underliggande benvävnad. Sjukdomen kan vara en följd av både en enda allvarlig intraartikulär skada och långvarig mikrotraumatisering av leden. Övervikt intar en särskild plats bland riskfaktorerna för utveckling av OA. Så hos kvinnor med fetma utvecklas artros i knälederna 4 gånger oftare jämfört med kvinnor med normal vikt. Man fann att övervikt inte bara är en riskfaktor för OA utan också bidrar till dess snabbare utveckling fram till funktionshinder. Förekomsten av sekundär artros har alltid en specifik orsak.
ETIOLOGI OCH RISKFAKTORER FÖR OSTEOARTHROSIS
Riskfaktorer för primär artros ■ Äldre ålder ■ Kvinnligt kön ■ Fysisk aktivitet ■ Övervikt ■ Tidigare skador ■ Hormonersättningsterapi ■ D-vitaminbrist ■ Rökning ■ Deformation av ledytor ■ Svaghet i quadriceps femoris muskel, intensiv fysisk aktivitet Orsaker till sekundär artrosutveckling ■ Posttraumatisk ■ Medfödd , förvärvade sjukdomar eller endemiska sjukdomar: Perthes sjukdom, hypermobilitetssyndrom, etc. ■ Metaboliska sjukdomar: ochronos, hemokromatos, Wilsons sjukdom, Gauchers sjukdom ■ Endokrinopatier: akromegali, hyperparatyreoidism, diabetes mellitus, hypotyreos ■ Kalciumdepositionssjukdom ■ Nephropatier (Charcot sjukdom)
Ledbrosk är en mycket specialiserad vävnad som består av en matris som innehåller två huvudmakromolekyler - glykosaminoglykaner (proteoglykaner) och kollagen - och kondrocyter nedsänkta i matrisen. Normalt är syntesen och nedbrytningen av brosk i leden i ett balanserat tillstånd. Men under påverkan av olika riskfaktorer störs denna balans, vilket leder till att processerna för destruktion av broskvävnad börjar fortgå snabbare än återhämtningsprocesserna. Sedan börjar en ond cirkel: förstörelsen av brosk leder till inflammation, som i sin tur intensifierar de destruktiva processerna i leden. För närvarande antas det att den inledande rollen i utvecklingen av OA tillhör det subkondrala benet: mikrofrakturer av trabeculae och cytokinproduktion utlöser broskskador.
Den höga koncentrationen av proteoglykaner i matrisen säkerställer en jämn fördelning av belastningen, vilket påverkar brosket och återställer formen efter avslutad belastning. Med en minskning av mängden glykosaminoglykaner minskar broskmatrisens motstånd mot fysisk stress och broskytan blir känslig för skador.
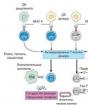
PATHOGENES AV OSTEOARTHROSIS
Etiologiska faktorer (genetiska, mekaniska etc.)
Dysfunktion hos kondrocyter
Överproduktion av cytokiner (K-1p, TNF-a), överuttryck av COX-2, transkriptionsfaktor NF-kB, nedsatt syntes av TGF-p
Enzymaktivering i synovialvätska
Nedbrytning av proteoglykaner och kollagen
Utbildning
antikroppar mot kollagen och proteoglykaner
Subchondral benrenovering
Artros
Dysfunktion
De viktigaste kliniska manifestationerna av artros är smärta och deformitet i lederna. Sjukdomen börjar med uppkomsten av mild smärta i lederna som upplever störst stress (knä, höft, metatarsofalangeal led i första tån). Först påverkas en led, sedan går andra med. Med utvecklingen av den patologiska processen uppträder smärta inte bara efter fysisk ansträngning utan också på natten, så kallad. meteosensitivity - en förändring i intensiteten av smärta beroende på temperatur, fuktighet och atmosfärstryck, vilket påverkar trycket i ledhålan. När OA fortskrider kan smärta uppstå (eller förvärras) med förändringar i kroppsläge, att gå upp från en stol eller gå ner. Utseendet på smärta på natten indikerar en aktiv
KLINISK BILD OCH STEG AV OSTEOARTHROSIS
Ledvärk
Crepitus i den drabbade leden
Den kliniska bilden av OA
Deformation av lederna
Begränsning av rörligheten i den drabbade leden
syn på inflammation i leden. Smärta kombineras ofta med morgonstyvhet och crepitus i den drabbade leden kan noteras. Utvecklingen av synovit åtföljs av svullnad i leden, en ökning av hudtemperaturen över den. Med uppkomsten av reflexmuskelkramper kan rörelsebegränsning i den drabbade leden uppstå, fram till bildandet av sen-muskelkontrakturer. Med en lång sjukdomsförlopp uppträder Heberden-noduler på de distala interfalangeala lederna, Bouchards noduler - på de proximala interphalangeal-lederna samt på de första metatarsophalangeal-, knä- och andra lederna.
Stadier av artros (enligt J. Kellgren och J. Lawrence, 1952)
0 - inga radiologiska tecken
1 - tvivelaktiga radiologiska tecken
II - minimala förändringar (lätt förminskning av artikulären
sprickor, enstaka osteofyter)
III - måttliga manifestationer (måttlig förträngning av artikulären
sprickor, flera osteofyter)
IV - uttalade förändringar (det gemensamma utrymmet är nästan inte spårbart
levande avslöjas grova osteofyter)
Förloppet för artros är varierande. I vissa fall, trots utvecklingen av röntgenmanifestationer av sjukdomen, förblir patientens tillstånd stabilt under många år. Smärtan ökar gradvis mot bakgrund av utvecklingen av deformitet och stelhet i lederna. Begränsningen av rörelserna i lederna under lång tid är fortfarande inte så betydelsefull. Under inflytande av provokerande faktorer (kylning, luftvägsinfektion) uppstår regelbundet reaktiv synovit, vars återfall blir vanligare med sjukdomsförloppet. Vid svår osteoartros kan ledblockeringar uppstå.
Artros kännetecknas av en snabb generalisering av processen och osteoartikulär förstörelse (erosiv artros). Denna kurs observeras oftare vid polyosteoartrit med närvaron av Heberden's knölar och en ärftlig benägenhet, liksom hos kvinnor under klimakteriet.
Hos män med en kraftfullare ligament-muskulös apparat finns det ett lättare förlopp av artros. De har episodiska polyarthralgier med mindre och långsamt progressiva radiologiska förändringar.
ALTERNATIV FÖR OA-KURS OCH LOCALISERING AV GEMENSAMMA LESIONER
ALTERNATIV FÖR OSTEOARTHROSIS KURS
Lokaliserad OA:
■ Handfogar
■ Fotfogar
■ Knäleder
■ Höftled
■ Ryggrad
■ Andra fogar
Generaliserad OA (3 grupper av leder eller mer):
■ med skador på de distala och proximala interfalangeala lederna
■ med skador på stora fogar
■ erosiv
Förekomst av olika lokaliseringar av OA i befolkningen *
Jag | Knäled (gonartros) I I Höftled (coxartros) I I Hand- och handledsfogar I I Fotled I I Övriga leder ** □ Nej OA
Invånare i Storbritannien som är 45 år och äldre som söker hjälp för osteoatros
** Inklusive OA av två eller flera leder av olika lokaliseringar
DIAGNOSTIK OSTEOARTHROSIS
Diagnosen av artros kan fastställas på grundval av närvaron av karakteristiska kliniska symtom, radiologiska tecken (förträngning av ledutrymmet, utplattning av ledhuvudet och glenoidhålan, närvaron av subkondral osteoskleros, uppkomsten av benväxter längs kanterna på ledytorna - marginella osteofyter). Informativa metoder för diagnos av sjukdomar
artroskopi, datortomografi, magnetisk resonanstomografi ingår också. Man bör komma ihåg att kliniska symtom inte alltid korrelerar med data om röntgen i lederna, magnetisk resonanstomografi, ultraljudsmetoder samt med makro- och mikroskopiska indikatorer som erhållits under artroskopi eller synovial biopsi.
Många röntgenpositiva patienter har inga kliniska symtom på OA, tvärtom: med en uttalad klinisk bild av sjukdomen kan röntgenegativitet observeras.
Till skillnad från artrit är ett fullständigt blodtal normalt, men med synovit kan ESR öka till 25 mm / h, fibrinogen ökar något. Synovialvätskan är transparent, antalet celler är mindre än 2000 mm3.
Neurologens konsultation
R-grafik av ryggraden
Dispensary observation
Ingen gemensam patologi
Inga kliniska tecken på OA, men neurologiska symtom (smärta)
Inga radiografiska bevis för gemensam OA
Inga sonografiska tecken
Ingen biokemisk
förändringar karakteristiska för OA
Inga immunförändringar som är karakteristiska för OA
Undersökning och undersökning av ortoped
R-grafi av höft- och knälederna
höft- och knäleder
Biokemisk undersökning av urin och blod
Immunologisk forskning
Avsedd synovit, smärta vid rörelse i extrema amplitudpositioner
Skleros, osteoporos, subkondrala bencyster, osteofyter
Synovit, kapselförtjockning, induration och annuluscyster
I blodet - en brist på GAG, i urinen - en ökning av fragment av GAG och kollagen
Ökade nivåer av CD3-CD16 + CD56 +, CD3 + CD25 +, CD3 + HLA-DR +, CEC, TNF-a
KLINISK INSTRUMENTAL DIAGNOSTIK OSTEOARTHROSIS
Kliniska symptom Objektiva tecken
Ledvärk
■ Ökad smärta under träning och minskad i vila
■ Morgonstyvhet (upp till 30 minuter)
■ Smärta vid palpering av lederna, passiva och aktiva rörelser
■ Krossande leder vid rörelse
■ Begränsa rörelsens omfång
■ Svullnad i lederna
■ Deformation / deformation av lederna (inklusive närvaron av Geberden och Bouchards knölar)
Röntgen tecken
■ Begränsning av fogutrymmet
■ Osteofyter
■ Subkondral skleros
Det rekommenderas att minska belastningen på de drabbade lederna: det rekommenderas inte att gå länge eller bära vikter. Användningen av en sockerrör och ett stöd, justerbar i höjd, kryck vid gång minskar belastningen på höftledet avsevärt.
Om du är överviktig rekommenderas dietterapi. Målet är att uppnå ett kroppsmassindex på 18,5 till 25 kg / m2. Du bör minska mängden fett i maten, öka konsumtionen av fisk, färska grönsaker och frukt. Menyn bör innehålla livsmedel med mycket fiber och livsmedel som innehåller svavel.
Fysiska övningar bör utföras utan statisk belastning (sittande, liggande, i poolen), långsamt, smidigt, med en gradvis ökning av belastningen, 10-15 minuter flera gånger under dagen (30-40 minuter om dagen).
Vid artros i knälederna är huvudövningarna övningar som hjälper till att stärka lårmusklerna (till exempel, lyft ett rakt ben i ryggläge och håll det i flera sekunder); övningar som syftar till att öka rörelseområdet ("cykel");
Icke-farmakologiska metoder för terapi av osteoartros
Minska stress på de drabbade lederna
■ Dietterapi (viktminskning minskar stressen på de drabbade lederna)
■ Begränsning av bärvikter
■ Använda en käpp eller stödkryka
Behandling och profylaktiska effekter
■ Sjukgymnastikövningar
■ Doserad fysisk aktivitet
Kirurgiska korrigeringsmetoder
■ Artroplastik
■ Fogens endoprotetik
övningar för att förbättra kroppens allmänna aeroba tillstånd (gå på plan terräng i måttlig
tempo). Gånglängden bör ökas gradvis till 30-60 minuter 5-7 dagar i veckan.
Läkemedelsbehandling för artros syftar till att undertrycka smärta och normalisera de drabbade ledernas funktion.
Läkemedlen som används för OA är indelade i två huvudgrupper: snabbverkande och långverkande symptommodifierande läkemedel. Den första gruppen inkluderar icke-steroida antiinflammatoriska läkemedel (NSAID), smärtstillande medel (enkla och opioida), muskelavslappnande medel och glukokortikoider. För att minska smärta, ledsvullnad och stelhet används paracetamol, indometacin, diklofenak, meloxikam, ibuprofensalva, tramadol.
Bland läkemedlen i den andra gruppen (symptommodifierande läkemedel med fördröjd verkan) tillhör den primära rollen de naturliga komponenterna i broskmatrisen - kondroitinsulfat och glukosamin, som är de mest studerade bland läkemedel i denna grupp.
MEDICINSK TERAPI AV OA
Läkemedelsgrupper Läkemedel Biverkningar
NSAID Indometacin, diklofenak, meloxikam Risk för gastropati, kardiovaskulära komplikationer
Muskelavslappnande medel Succinylkolin Bradykardi, hypotoni, fascikulationer, ökat ögontryck, malign hypertermi
Glukokortikosteroider Prednisolon, dexametason, metylprednisolon Ulcerogen verkan, steroiddiabetes, Itsenko-Cushings syndrom, osteoporos, etc.
Långsamverkande symptommodifierande läkemedel Kondroitinsulfat, glukosamin Ej uttryckt
Dessa läkemedel saktar ner utvecklingen av OA, förhindrar nedbrytning av brosk, förhindrar utveckling av OA i intakta leder,
vilket gör att vi kan betrakta dem som läkemedel med patogenetisk verkan vid behandling av osteoartros.
Kondroitinsulfat (CS) - en av de viktigaste grundkomponenterna i bindväv, är en del av ben, brosk, senor, ligament, ger till stor del den mekaniska funktionen hos leden, särskilt motstånd mot kompression. Artros är associerad med lokal brist på vissa ämnen, inklusive kondroitinsulfat, därför är dess användning i OA rimlig. CS har en antiinflammatorisk effekt, stimulerar syntesen av proteoglykaner, kollagen och hyaluronsyra, minskar kondrocyternas kataboliska aktivitet och påverkar metabolismen av det subkondrala benet. Det har bevisats att biologisk CS-aktivitet utförs genom att verka på NF-kB (en av huvudregulatorerna för det inflammatoriska svaret), minska uttrycket av IL-ip av kondrocyter och synoviocyter, minska koncentrationen av proinflammatoriska molekyler (CRP, IL-6), hämma uttrycket av COX-2.
Klinisk farmakokinetik för CS
När det tas per os adsorberas läkemedlet snabbt från mag-tarmkanalen och kommer in i den systemiska cirkulationen
KONDROITINSULFAT I OA-TERAPI
Bevisbas för kondroitinsulfat
Forskningsresultat
Analys av Schneider H. et al. (2012) med hjälp av databaser MEDLINE, Cochrane Register och EMBASE. Analyserade 3 studier med adekvat design (5 poäng på en skala 1a (1f. Studierna inkluderade 588 patienter med knäleds OA, 291 av dem tog CS och 297 - placebo. Resultaten av studierna bekräftade, att CS i en dos av 1 g / dag minskar smärtintensiteten avsevärt och förbättrar det funktionella tillståndet i lederna.
Forskning av Michel et al. (2005) Observation av 300 patienter med gonartros under 2 år avslöjade en signifikant stabiliserande effekt av kolesterol på bredden av ledutrymmet, vilket bromsar utvecklingen av OA.
STOPP-studie (fahan A. et al.) (2009) Studien inkluderade 622 patienter med gonartros. I huvudgruppen registrerades en mindre uttalad förträngning av fogutrymmet jämfört med kontrollgruppen (-0,07 respektive 0,31 mm, p< 0,0005) и меньшее число больных с рентгенологическим прогрессированием ^ 0,25 мм по сравнению с плацебо (28 против 41%; р < 0,0005).
huvudsakligen lågmolekylära derivat upp till 90% av den dos som tas och 10% av nativa molekyler. Biotillgängligheten av kolesterol är i genomsnitt 10 till 20%. Den maximala koncentrationen av kolesterol i blodet uppnås 3-4 timmar efter administrering och i synovialvätskan - efter 4-5 timmar Kolesterol utsöndras huvudsakligen av njurarna.
Kliniska och farmakologiska effekter av kolesterol
■ Förbättrar trofism av benvävnad.
■ Minskar benresorption.
■ Förbättrar elasticiteten i det intraartikulära brosket.
Glukosamin är en monosackarid och en naturlig komponent i glykosaminoglykanerna i ledmatrisen och synovialvätskan. Det finns flera glukosaminsalter, glukosaminsulfat och glukosaminhydroklorid används som läkemedel. Bevisbasen är glukosaminsulfat.
Klinisk farmakokinetik för glukosamin
Den orala biotillgängligheten för glukosamin är 25%. När glukosaminsulfat tas i terapeutiska doser kommer glukosamin in i både plasma och synovialvätska, medan koncentrationen av läkemedlet i synovialvätskan är 3,22-18,1 μmol / dl. Halveringstiden för glukosamin är cirka 15 timmar.
Kliniska och farmakologiska effekter av glukosamin
■ Stimulerar syntesen av kondrocyter av högkvalitativ extracellulär matris (proteoglykaner och hyaluronsyra)
GLUKOSAMIN I OA-TERAPI
Bevisbas för glukosaminsulfat
Forskningsresultat
Towheed T.E. et al. (2005), Cochrane Database of Systematic Reviews Effektiviteten av glukosaminsulfat (GS) är signifikant högre än placebo när det gäller att minska intensiteten i ledvärk, förbättra ledarnas funktionella tillstånd, bedömt med Lequesne-index. Bland patienter som tog GS var det en högre andel patienter som svarade på behandlingen
Reginster J.Y. et al. (2001) 212 patienter med gonartros randomiserades i två grupper: de tog glukosaminsulfat eller placebo i tre år. Fogutrymmets bredd ökade med 0,12 mm i slutet av studien, i placebogruppen minskade den med 0,24 mm
Pavelka K. et al. (2002) 202 patienter med OA i knäleden (genomsnittlig ledutrymmesbredd på cirka 4 mm, ett värde på Leeken-skalan på högst 9 poäng) randomiserades till GS- och placebogrupperna. Efter 3 års uppföljning minskade ledutrymmets bredd med 0,19 mm hos patienter i placebogruppen, i gruppen som fick GS - ökade med 0,04 mm
■ Minskar pålitligt aktiviteten hos kataboliska enzymer i brosk, inklusive matris-MMP, undertrycker synkronisering
avhandling av kväveoxid, stimulerar syntesen av kondroitinsvavelsyra.
Teraflex (Bayer) är ett av de mest kända kombinerade läkemedlen med beprövad hondroprotektiv aktivitet. Teraflex innehåller 500 mg glukosaminhydroklorid och 400 mg kondroitinsulfat. Kombinationen av de två huvudkondroprotektorerna ger förstärkning av den positiva effekten av var och en av dem, eftersom kondroitinsulfat och glukosamin är synergistiska, kompletterar och förstärker varandras verkan. I ett experiment med OA-modellen hos kaniner visades det att kombinerade läkemedel ökar syntesen av glukosaminoglykaner av kondrocyter med 96,6%, och mot bakgrund av monoterapi med symtommodifierande läkemedel med försenad verkan - endast med 32%.
Det ordineras 3 kapslar per dag under de första 4 veckorna, sedan 2 kapslar per dag. Antagningstiden bör vara minst 6 månader. Läkemedlets effektivitet ökar med dess långvariga användning (många månader och många år). Med tanke på förekomsten av läkemedlet efterverkan kan det ordineras genom upprepade 6-månaders kurser följt av en paus i 3-6 månader.
Teraflex har antiinflammatoriska, smärtstillande och hondroprotective effekter, vilket framgår av resultaten av många studier.
DET KOMBINERADE TILLVERKNINGSTERAFLEXEN I TERAPI AV OSTEOARTHROSIS
Kliniska och farmakologiska effekter av Teraflex:
■ Har antiinflammatoriska och smärtstillande effekter
■ Stimulerar bildandet av hyaluronon, syntesen av proteoglykaner och kollagen typ II
■ Undertrycker aktiviteten hos enzymer som bidrar till nedbrytningen av brosk
■ Stimulerar regenerering av broskvävnad
■ Saktar ned hastigheten för artros
Indikationer av läkemedlet Teraflex
Degenerativ-dystrofiska sjukdomar i leder och ryggrad:
■ artrossteg 1-111
■ osteokondros
Evidensbas för kombinationen kondroitin och glukosamin (inklusive Teraflex)
Studie
Analys av McAlindon et al. (2000)
Das A. Jr. et al. GAIT-studie (glukosamin / kondroitin artritinterventionstest) (2000)
Research Institute of Reumatology, Russian Academy of Medical Sciences (2008).
resultat
En metaanalys av 15 dubbelblinda, placebokontrollerade studier av effekten av glukosamin och kondroitinsulfat utfördes. Bevisade effektiviteten av glukosamin och kondroitinsulfat som symtomatiska medel
(minskar smärta och förbättrar funktionell status) vid behandling av artros i knä- och höftlederna
Effekten av glukosamin, kondroitinsulfat och deras kombination studerades hos 1 583 patienter med knä-OA. Det visade sig att hos patienter med intensivt smärtsyndrom var effektiviteten av kombinationsbehandling (kondroitinsulfat och glukosaminhydroklorid) signifikant högre jämfört med placebo och monoterapi med dessa läkemedel.
Effekten av Teraflex utvärderades hos 100 patienter med gonartros: 50 patienter tog Teraflex dagligen i 9 månader. och 50 patienter i intermittent läge (3 månaders mottagning, 3 månaders ledighet, 3 månaders mottagning). Efter en niomånaders behandling bedömdes läkemedlets efterverkan i 3 månader. Analys av resultaten visade att intermittent terapi med Teraflex är lika effektiv vid konstant administrering av läkemedlet när det gäller dess effekt på smärta, ledfunktion och varaktigheten av efterverkan.
SLUTSATS
■ Artros tar ledande ställning bland sjukdomar i muskuloskeletala systemet. OA anses vara en kronisk progressiv sjukdom i de synoviala lederna som utvecklas som ett resultat av ett komplext komplex av biomekaniska, biokemiska och / eller genetiska faktorer. Kärnan i degenerativa dystrofiska förändringar i artros är den primära skadan på brosket, följt av en inflammatorisk reaktion.
■ De viktigaste grundläggande kondroskyddsmedlen vid behandling av artros är glukosaminsulfat / hydroklorid och kondroitinsulfat på grund av deras höga effektivitet, bevisat i kliniska studier och en optimal säkerhetsprofil. Kondroitinsulfat och glukosaminsulfat / hydroklorid har antiinflammatoriska och smärtstillande effekter, med långvarig användning saktar de ned utvecklingen av artros.
■ Teraflex är ett kombinerat kondroskyddande läkemedel som innehåller 500 mg glukosaminhydroklorid och 400 mg kondroitinsulfat. Teraflex-komponenter är synergistiska, förstärker och kompletterar varandras farmakologiska verkan. Forskningsresultat och erfarenhet av tillämpning gör det möjligt att betrakta Teraflex inte bara som ett symptommodifierande och strukturellt modifierande läkemedel utan också som ett medel för patogenetisk behandling av artros.
LITTERATUR
1. Kotelnikov G.P., Lartsev Yu.V. Artros: M.: Geotar-Media, 2009.
2. Kryukov N.N., Kachkovsky M.A., Babanov S.A., Verbovoy A.F. Terapeutens handbok. Rostov n / a: Phoenix, 2013.
3. Svetlova M.S. Gonartros i tidigt stadium: klinisk och instrumentell, laboratorieegenskaper och sjukdomsmodifierande terapi. Författarens abstrakt. diss. Dr. med. vetenskap. Yaroslavl, 2009.
4. Alekseeva L.I., Sharapova E.P. Kombinerade symtomatiska långverkande läkemedel vid behandling av artros. RMZh, 2009, 17 (4).
5. Alekseeva L.I. Kombinerade läkemedel vid behandling av artros. Medicinska rådet, 2012, 8.
6. Nasonova V.A. Artros är ett problem med polymorbiditet. Consilium medicum, 2009, 1: 5-8.
7. Kovalenko V.N., Bortkevich O.P. Artros. En praktisk guide. 2: a upplagan, Rev. och lägg till. K.: Morion, 2005.
8. Volpi N. Kondroitinsulfat för behandling av artros? Curr. Med. Chem., 2005,4: 221-34.
9. Chichasova N.V. Kondroitinsulfat (Structum) vid behandling av artros: patogenetisk effekt och klinisk effekt. RMZh, 2009, 17 (3).
10. HDchberg M. Struktureffekter av kondroitinsulfat vid knäartros: en uppdaterad metaanalys av randomiserad placebokontrollerad studie med två års varaktighet. Artros Brosk, 2010, 18: 28-31.
11. Zhang W, Nuki G, Moskowitz RW, et al. OARSI-rekommendationer för hantering av höft- och knäartros. Del III: förändringar i bevis efter systematisk kumulativ uppdatering av forskning publicerad till januari 2009. Artros Brosk, 2010, 18: 476-99.
12. Schneider H., Maheu E., Cucherat M. Symptommodifierande effekt av kondroitinsulfat i knäartros: En metaanalys av randomiserade placebokontrollerade försök utförda med Structum®. Öppna Rheumatol. J., 2012, 6: 183-189.
13. ^ han A. et al. Långsiktiga effekter av kondroitiner 4 och 6 sulfat på knäartros: Studien om förebyggande av osteoartrit, en tvåårig, randomiserad, dubbelblind, placebokontrollerad studie. Artrit Reum.2009, 60 (2): 524-533.
14. Towheed TE, Maxwell L. Anastassiades TP et al. Glukosaminbehandling för behandling av artros. Cochrane Database of Systematic Reviews, 2005.
15. Pavelka K, Gatterova J, Olejarova M et al. Användning av glukosaminsulfat och fördröjning av progression av knäartros: en 3-årig, randomiserad, placebokontrollerad, dubbelblind studie. Arch Intern Med 2002, 162 (18): 2113-23.
16. Reginster JY, Deroisy R, Rovati LC, et al. Långsiktiga effekter av glukosaminsulfat på artrosprogression: en randomiserad, placebokontrollerad klinisk studie. Lancet 2001, 357 (9252): 251-6.
17. Lippielo L, Woodword J, Karpman D et al. Gynnsam effekt av broskstrukturmodifierande medel testade i kondrocyt- och kanininstabilitetsmodell osteoartros. Arthr. Rheum 1999 suppl. 42: 256.
18. McAlindon TE, LaValley MP, Gulin JP, Felson DT. Glukosamin och kondroitin för behandling av artros: en systematisk kvalitetsbedömning och metaanalys. JAMA 2000,283 (11): 1469-1475.
19. Das A. Jr., Hammad T.A. Effekten av en kombination av FCHG49-glukosaminhydroklorid, TRH122 natriumkondroitinsulfat med låg molekylvikt och manganaskorbat vid hantering av knäartros. Artros Brosk, 2000, september, 8 (5): 343-350.
20. Alekseeva L.I., Kashevarova N.G., Sharapova E.P., Zaitseva E.M., Severinova M.V. Jämförelse av permanent och intermittent behandling av patienter med artros i knälederna med det kombinerade preparatet "Teraflex". Vetenskaplig och praktisk reumatologi, 2008, 3: 68-72.
21. Arthritis Research UK 2013, Artros i allmänpraxis.
27.03.2015
22 oktober 2003 vid institutet för kardiologi. N. D. Strazhesko AMS i Ukraina lanserade en tre dagars gemensam plenum för kardioreumatologer och ortopediska traumatologer i Ukraina "Konsensus om terminologi, nomenklatur, klassificering, program och standarder för behandling av ledsjukdomar." Denna händelse väckte stort intresse för medicinska kretsar, uppmärksammades av specialister inte bara från Ukraina utan också från andra länder.
En av de allmänna sponsorerna för plenum var det franska företaget EUROMEDEX. Med hennes stöd hölls ett symposium om användningen av en grupp läkemedel som är relevanta för artrologi - kondroprotektorer. Som professor V.N. Kovalenko, under lång tid var dessa läkemedel praktiskt taget frånvarande på den ukrainska marknaden, men nyligen har ett dussin kondroprotektorer med olika egenskaper dykt upp. Det enda läkemedlet som certifierats av FDA, USA, är Structum (kondroitinnatriumsulfat, 500 mg) tillverkat av Pierre Fabre, Frankrike. Ledande experter från Ukraina, Ryssland och Vitryssland berättar om sin första erfarenhet av att använda Structum i kliniken.
Den patogenetiska motivationen för användning av kondroprotektorer presenterades av doktor i medicinska vetenskaper, professor N.M.Shuba, chefreumatolog vid Ukrainas hälsovårdsministerium.
- Problemet med artros är för närvarande ett av de mest angelägna inom modern artrologi, främst på grund av den höga medicinska och sociala betydelsen. Artros är en grupp av polyetiologiska degenerativa ledsjukdomar med primär skada på ledbrosket. I den utländska litteraturen dominerar termen "artros" på grund av det faktum att den inflammatoriska komponenten spelar en viktig roll i sjukdomens patogenes.
Vid artros påverkas hela leden, nämligen: ledbrosk, subkondralt ben, synovium, ligament, kapsel och muskler. Med tanke på allt detta är patogenesen för artros ganska komplex.
Den patogenetiska underbyggnaden av kondroprotektorns roll vid artros är att klargöra de biologiska egenskaperna hos glykosaminoglykaner. En av dem är kondroitinsulfat, en sulfaterad glykosaminoglykan med en molekylvikt av 10-40 kDa. Dess huvudroll är att stödja hydratiseringen av brosket.
Särskild uppmärksamhet i modern artrologi ägnas åt kondroitinsulfat-4.6 (XC-4.6), registrerat i Ukraina som ett läkemedel Structum, vars produktion är certifierad av FDA, USA. De främsta fördelarna med Structum jämfört med andra kondroprotektorer är.
- Det är den enda kondroprotektorn som har certifierats av FDA, USA.
- Tillverkad på basis av fjäderfäsäkra råvaror som inte innehåller pationer av prioninfektioner, till skillnad från råvaror från nötkreatur.
- Den har låg molekylvikt, vilket beror på modern teknik med standardiserad molekylvikt.
- Mycket biotillgängligt i förhållande till brosk, vilket bekräftas in vivo och ex vivo.
- Tåls väl av patienter, har inga biverkningar.
- Har en hög grad av bevis.
- Rekommenderas för användning av EULAR (European Anti-Rheumatic League).
XC-4.6 har farmakokinetiska och farmakodynamiska egenskaper. Detta läkemedel absorberas i blodet med mer än 80%, en stabil koncentration i blodet bildas efter 14-18 timmar. Den extremt höga tropism av XC-4.6 till vävnader som är rika på glykosaminoglykaner bestämmer dess höga biotillgänglighet i förhållande till brosk och ben, uppgår till 13%.
Verkningsmekanismerna för XC-4.6 är flervägda.
- Läkemedlet stimulerar syntesen av transformerande tillväxtfaktor, kollagen, proteoglykaner och vävnadshämmare av metalloproteaser av kondrocyter.
- Det hämmar interleukin-1, prostaglandin E2, metalloproteaser (kollagenaser, stromelysin), tumörnekrotisk faktor-a, interleukin-6, γ-interferon.
- Kondroitinsulfat främjar syntesen av hyaluronsyra av kondrocyter, hämmar aktiviteten hos ett antal enzymer: elastas, tiolproteas, chymotrypsin, hyaluronidas.
- Läkemedlet påverkar synovialvätskans sammansättning, stimulerar införandet av glykosamin i hyaluronsyrafraktionen, vilket ökar viskositeten hos synovialvätskan, såväl som benmetabolism, vilket bidrar till bevarande av benkalciumreserver, stimulerar osteosyntes och benregenerering vid skada.
Följaktligen bevarar Structum broskmatrisen, upprätthåller synovialvätskehomeostas, hämmar det inflammatoriska svaret, minskar frekvensen och intensiteten av ledskador och främjar bildandet av brosk och benvävnad. Baserat på detta och med hänsyn till det stora spektrumet av verkan, hög effektivitet och säkerhet vid långvarig användning kan Structum tillskrivas de grundläggande läkemedlen med kondroskyddande verkan.
 En genomgång av den moderna läkemedelsbehandlingsstrategin för artros presenterades i rapporten från O. B. Yaremenko, doktor i medicinska vetenskaper.
En genomgång av den moderna läkemedelsbehandlingsstrategin för artros presenterades i rapporten från O. B. Yaremenko, doktor i medicinska vetenskaper.
- Oavsett vad som orsakade kränkningen av ledens biomekanik - ett brott mot den normala fördelningen av trycket på brosket och en ökning av belastningen på dess individuella delar eller cytokinberoende mekanismer för att öka ledbroskets katabolism - huvudproblemet med en sådan sjukdom som artros är strukturell och funktionell skada på broskvävnaden. Detta återspeglas i de många definitionerna av artros, både inhemska och utländska.
Följaktligen är huvudmålet för behandling av artros att sakta ner de strukturella och funktionella förändringarna i brosk, det vill säga den maximala möjliga hämningen av den destruktiva processens utveckling. Ett sekundärt mål, även om det är ett primärt mål för patienten, är att minska smärta och inflammation.
1994 föreslog WHO-experter en klassificering av läkemedel som används för degenerativa ledsjukdomar, som stöddes av American College of Rheumatology samma år och 1996 av European League of Antirheumatica (EULAR). Enligt denna klassificering finns det tre grupper av läkemedel.
- Snabbverkande symtomatiska läkemedel - NSAID, paracetamol och centrala analgetika (tramadol). Effekten av deras användning sker inom flera dagar och försvinner efter att läkemedlet har avbrutits. Glukokortikoider i form av intraartikulära injektioner kan också hänvisas till symtomatiska snabbverkande läkemedel.
- Långsamverkande symtomatiska läkemedel, vars effekt manifesteras inom 1-3 månader från behandlingsstart och kvarstår under en tid efter utsättande. Dessa inkluderar: kondroitinsulfat, glykosaminsulfat, hyaluronsyra, diacerein.
- Preparat som modifierar broskstrukturen. 1994 visade inget av läkemedlen de egenskaper som skulle göra det möjligt att tillskriva det så kallade kondromodifierande läkemedlen (kondroprotektorer).
Sådana läkemedel som rumalon, arteparone, alflutop bör endast nämnas i en historisk aspekt. Det finns många anledningar till detta, varav det huvudsakliga är en mycket svag evidensbas för deras effektivitet.
Det första långsamma läkemedlet som presenteras på läkemedelsmarknaden i Ukraina är Structum (kondroitinsulfat-4,6). Enligt experimentella studier bestäms detta läkemedel efter en enstaka dos efter 1, 2 och 3 dagar i kroppen, ackumuleras i vävnaderna i muskuloskeletala systemet, nämligen i ledbrosk och ledvätska. Detta ökar broskets elastiska elastiska egenskaper. Dessutom, som redan nämnts, har detta läkemedel ett antal anti-kataboliska och anabola effekter, hämmar inflammation och stimulerar syntesen av proteoglykaner av kondrocyter.
Effektiviteten av Structum har utvärderats i ett antal kliniska prövningar. Enligt en metaanalys av de sju mest omfattande studierna, efter 2-3 månaders användning av Structum, observeras en minskning av smärtsyndromet, efter en månad (30-40 dagar) minskar behovet av NSAID signifikant.
En viktig egenskap hos Structum är bevarandet av den uppnådda terapeutiska effekten efter utsättning av läkemedlet i flera månader. Varaktigheten av eftereffekten beror på varaktigheten av behandlingen.
År 2000 analyserade experter från European Antirheumatic League effektiviteten av läkemedel som används för att behandla artros. Det visade sig att kondroitinsulfat har en effekt som överstiger effekten av arteparon (8 gånger), hyaluronsyra (2 gånger), diklofenak (2 gånger).
I en av studierna visade det sig att efter två tre månaders behandlingskurser med Structum sågs inte förträngningen av ledutrymmet hos patienter, till skillnad från patienter som fick placebo.
Dessa data indikerar att Structum är en verklig konkurrent för dess inkludering i gruppen av kondromodifierande läkemedel för behandling av artros. Denna ståndpunkt återspeglas i rekommendationerna från European Antirheumatic League 2000, där det noteras att läkemedel som kondroitinsulfat, hyaluronsyra, glykosaminsulfat, diacerein kan ha strukturmodifierande egenskaper. För närvarande är det mest bevis som stöder användningen av dessa två läkemedel kondroitinsulfat och glykosaminsulfat. Det finns få eller inga tecken på effekt för resten av denna grupp läkemedel.
Återigen vill jag betona att huvudmålet med artrosbehandling är att bevara broskvävnad. Jämför effekten av olika läkemedel på sjukdomsförloppet, bör man vara uppmärksam på de av dem som har en bevisad positiv effekt på metabolismen av brosk och på det radiografiskt bekräftade bevarande av ledvävnadens struktur. Sådana läkemedel är diacerein, kondroitinsulfat, glykosaminsulfat. Icke-steroida antiinflammatoriska läkemedel och glukokortikoider påverkar antingen inte dessa indikatorer eller har en negativ effekt.
Sammanfattningsvis kan vi dra slutsatsen att från spektrumet av för närvarande existerande läkemedel för behandling av artros, är det lämpligt att använda strukturmodifierande läkemedel, varav det mest effektiva enligt experimentella och kliniska studier var kondroitinsulfat-4.6 (Structum). Patienter som inte kan tolerera kondroitinsulfat visas artikulära injektioner av hyaluronsyra, och en alltmer cool inställning bildas gentemot den senare i vetenskapliga kretsar, eftersom det finns bevis för den negativa effekten av injektioner på broskmetabolismen, liksom att läkemedel som injiceras direkt i leden är mer än i 30% av fallen kommer de inte in i dess hålighet, men införs i de periartikulära vävnaderna. När det gäller snabbverkande läkemedel, bör de användas så sällan som möjligt, särskilt för NSAID; det är tillrådligt att använda dem bara tills effekten av långsamt verkande läkemedel uppträder.
 Professor L. I. Alekseeva (Ryssland, Moskva) presenterade symposiedeltagarnas uppmärksamhet resultaten av mångfacetterade studier av Structums kliniska och ekonomiska effektivitet vid behandling av artros.
Professor L. I. Alekseeva (Ryssland, Moskva) presenterade symposiedeltagarnas uppmärksamhet resultaten av mångfacetterade studier av Structums kliniska och ekonomiska effektivitet vid behandling av artros.
- Artros är en allvarlig, handikappande sjukdom som förtjänar särskild uppmärksamhet från kliniker. De ledande symptomen på artros är smärta och dysfunktion i lederna. Detta är den vanligaste sjukdomen som påverkar lastlederna - knä, höft och intervertebral, vilket leder till djup funktionshinder hos patienter.
Artros anses nu vara en organpatologi, med tanke på att alla ledvävnader påverkas. Jag vill betona att artros inte betraktas som en slitage på ledytorna under åldrandet, utan som en metabolisk sjukdom. Den avgörande faktorn i patogenesen för denna sjukdom anses vara kränkning av syntes och reparation i alla vävnader i leden - först och främst i broskmatrisen såväl som i det subkondrala benet och omgivande vävnader.
För en bättre förståelse av de grundläggande principerna för modern terapi av artros är det nödvändigt att komma ihåg kondroitinsulfats roll i broskvävnad. Att vara en av komponenterna i broskmatrisen och har anjoniska egenskaper, ger kondroitinsulfat broskens elasticitet. När brosket laddas konvergerar kedjorna av kondroitinsulfat och förflyttar vatten från matrisen till broskytan, vilket i sig själv underlättar fogens arbete på grund av smörjning av ledytorna. Efter laddning återgår de negativt laddade kedjorna av kondroitinsulfat till sin tidigare position, vilket underlättas genom kvarhållande av proteoglykan av kollagenfibrer. Således fungerar en välkoordinerad mekanism som gör att du kan motstå belastningen.
Artros är en sjukdom som orsakas av olika etiologiska faktorer som bidrar till klyvning av broskmatrisen av enzymer. Skräp från nedbrutna matrixkomponenter (proteoglykaner och kollagen) släpps ut i synovialvätskan och orsakar sekundär inflammation. Gradvis skiftar den metaboliska balansen mot övervägande av katabolism framför anabolism, det vill säga utvecklingen av broskförstörelse utan adekvat reparation, vilket leder till fiberdisformering av broskvävnaden och sekundär synovit.
År 1994 samlades en arbetsgrupp av forskare för att studera artros i USA, vid det sista mötet, där man beslutade att artros inte är en rent inflammatorisk sjukdom utan en sjukdom med inflammationsepisoder. De inflammatoriska reaktionerna som observerats i synovium liknar faktiskt mycket reumatoid artrit, men förekommer endast vid fästningsstället för synovialmembranet till brosket och har en periodicitet. Resultatet av artros är djupgående radiologiska förändringar när ledens struktur och funktion förloras.
Om målet tidigare med farmakoterapi mot artros ansågs minska smärta, inflammation och återställa ledfunktionen, är nu huvuduppgiften att bromsa utvecklingen av den destruktiva processen.
Jag presenterar resultaten av kliniska studier av vissa läkemedel som har fått status som strukturmodifierande i förhållande till ledbrosk (kondroitinsulfat, dess glykosamin, cytokinmodulatorer, piascledin (en icke-förtvålande förening av avokado-soja), andra hämmare av metalloproteinaser, hyaluronsyra. ges till kondroitinsulfat, registrerat som Structum från Pierre Fabre, av följande skäl.
Även om kondroitinsulfat spelar en viktig roll i strukturen av brosk (ger det elasticitet, ger smörjning av ledytorna under belastning på leden), är dess användning för behandling av artros främst på grund av effekten på broskmetabolismen - det vill säga anabol verkan med samtidig hämning av kataboliska processer, och särskilt - cytokinoberoende hämning av proinflammatoriska mediatorer. Särskilt viktigt i verkningsmekanismen för Structum är att det avbryter interleukin-1-beroende hämning av enzymer. Denna kvalitet skiljer den från glykosaminsulfat. Därför valdes Structum för mångfacetterade studier som ett läkemedel som har kraftfulla verkningsmekanismer på olika länkar i patogenesen för artros.
Jag gör er uppmärksam på resultaten av metaanalyser av andra författares studier och data från min egen forskning.
De behandlingsstandarder som har skapats de senaste åren ger en speciell kolumn - bevisnivån. Bevisbaserad medicin får mer och mer vikt vid bedömningen av läkemedlets effektivitet. En av metoderna för evidensbaserad medicin är metaanalys - en systematisk genomgång av arbeten med statistiska metoder, på grundval av vilka resultaten från flera studier sammanfattas.
För en metaanalys av effektiviteten i användningen av Structum tog vi fyra studier, under vilka följande bevisades separat.
- Kondroitinsulfat minskade smärtan jämfört med placebo;
- 65% av patienterna som fick detta läkemedel noterade en förbättring av deras tillstånd jämfört med kontrollgruppen.
- Läkemedlet kan minska funktionsnedsättningen jämfört med placebo.
- Biverkningarna med läkemedlet var desamma jämfört med placebo eller var frånvarande.
En annan metaanalys samlade data från separata studier som visade att kondroitinsulfat har en uttalad effekt, men dessa studier genomfördes under åren.
En negativ aspekt som påverkar studiens kvalitet och fullständighet är varaktigheten för patientobservation, eftersom artros är en långsamt progressiv sjukdom. Under normala förhållanden sker förträngningen av ledutrymmet endast med 0,3 mm per år, så för att bevisa den strukturmodifierande effekten av läkemedel vid osteartrit måste patienter observeras i minst två år.
För närvarande finns det två verk med övertygande beprövad strukturmodifierande effekt av läkemedlet Structum. Hos en av dem observerades 300 patienter som fick 800 mg kondroitinsulfat dagligen i två år. Tydliga data erhölls om att de drabbade knäledernas ledutrymme förblev oförändrat, det vill säga, medan man tar kondroitinsulfat noterades en stabilisering av den degenerativa processen, medan hos patienter som fick placebo avslöjades en minskning av ledutrymmet.
Det andra arbetet utfördes med deltagande av 115 patienter och avsåg den nodulära formen av artros. Bokföringen utfördes inte av storleken på det gemensamma utrymmet utan av antalet bildande av nya Heberden-knölar under en treårsperiod. En sådan långtidsstudie visade att patienter som tog Structum hade signifikant färre nybildade knölar jämfört med kontrollgruppen.
Därför är det nödvändigt att revidera metoden för att använda Structum till förmån för dess tidigaste recept och längre användning, eftersom systematiska granskningar och metaanalyser av studier har visat dess säkerhet och ganska hög effekt hos patienter med artros, pålitligt avslöjade förekomsten av läkemedlets strukturmodifierande egenskaper.
En rad studier har genomförts vid vårt institut. En av dem var öppen, randomiserad och jämförde den kliniska effekten av Structum och ibuprofen. En multicenterstudie genomfördes där 555 patienter från nio centra i Ryska federationen deltog. Vi fick samma resultat som tidigare författare. Structum minskade tydligt artikulärt syndrom, smärta, ökad funktionsförmåga och gjorde det också möjligt att minska dosen läkemedel som används som samtidig behandling, särskilt IVC-läkemedel. Den genomsnittliga dosen av att ta NSAID medan du tog Structum och efter dess avbrytande var lägre än i kontrollgruppen.
En uttalad eftereffekt av Structum avslöjades också. Patienterna undersöktes ett år efter avslutad behandling, dynamiken i det funktionella Lequesne-indexet hos patienter med gonartros, liksom hos patienter med coxartros, återgick inte till den initiala nivån, till skillnad från patienter som behandlats med icke-steroida antiinflammatoriska läkemedel.
Biverkningar under ett och ett halvt år av Structum-användning inträffade mycket mindre ofta än hos patienter som tog NSAID, vilket verkligen är viktigt, eftersom det förbättrar patienternas livskvalitet och inte kräver extra dyr behandling.
Dessutom analyserade vi antalet förvärringar av ostearthrosis, antalet sjukhusvistelser och polikliniska besök hos patienter och antalet dagar av funktionshinder och avslöjade en signifikant minskning av dessa indikatorer hos patienter som tog Structum jämfört med kontrollgruppen. Denna studie bekräftar inte bara en höjning av livskvaliteten för en patient med artros utan visar också de ekonomiska fördelarna med att använda Structum - både för patienten själv och för staten.
Vi analyserade också effekten av Structum-applikation på förloppet av samtidiga sjukdomar. En signifikant minskning av antalet förvärringar av kroniska sjukdomar i mag-tarmkanalen, liksom andra samtidigt patologier, avslöjades. Data om förbättringen av förloppet av arteriell hypertoni och ischemisk hjärtsjukdom när Structum användes i jämförelse med kontrollgruppen var oväntat för oss.
På grund av det faktum att nyligen ett av de viktiga kraven för läkemedel är bekräftelse av inte bara läkemedlets kliniska effekt och säkerhet utan också dess ekonomiska effektivitet, genomfördes en oplanerad ekonomisk analys baserad på resultaten av en studie om användningen av läkemedlet Structum. Trots den relativt höga kostnaden för Structum har terapi med detta läkemedel en högre kostnadseffektivitet än traditionell NSAID-behandling, med hänsyn till behandlingen av biverkningar.
Baserat på de presenterade uppgifterna kan det hävdas att Structum är ett mycket effektivt läkemedel för behandling av artros, har en lång efterverkan, minskar antalet förvärringar av sjukdomen, frekvensen av sjukhusvistelser och antalet dagar med funktionshinder, samt behovet av icke-steroida antiinflammatoriska läkemedel och förbättrar förloppet för vissa samtidiga kroniska sjukdomar.
 Doktor i medicinska vetenskaper, professor N.F. Soroka (Vitryssland, Minsk) ägde en rapport åt den farmakoekonomiska bedömningen av effektiviteten hos Structum hos patienter med artros baserat på sin egen forskning.
Doktor i medicinska vetenskaper, professor N.F. Soroka (Vitryssland, Minsk) ägde en rapport åt den farmakoekonomiska bedömningen av effektiviteten hos Structum hos patienter med artros baserat på sin egen forskning.
- Syftet med vår studie var att bestämma Structums ekonomiska effektivitet. Detta behov uppstod på grund av att läkemedlet är både mycket effektivt och ganska dyrt, så det var nödvändigt att avgöra om dess användning var ekonomiskt motiverad.
Studien utfördes i en vanlig poliklinik i Minsk, arbetet utfördes av en reumatolog. Studien involverade 100 patienter, utvalda för följande kriterier:
- med en tillförlitlig diagnos av artros;
- mellan 45 och 60 år;
- arbetande patienter;
- artros steg I - III enligt Kelgren;
- patienter som dagligen upplevde ledvärk, för vilka de tvingades använda NSAID;
- på en visuell analog skala (VAS) är svårighetsgraden av smärta mer än 40 mm.
Patienter uteslöts från studien, respektive:
- med en tvivelaktig diagnos;
- under 45 eller över 60;
- med allvarliga samtidigt sjukdomar;
- sex månader eller mindre före studien som fick annan antiartritbehandling;
- som använde glukokortikosteroider intraartikulärt;
- icke-arbetande patienter.
100 patienter randomiserades i två grupper. Patienterna i den experimentella gruppen fick NSAID, sjukgymnastikbehandling och Structum. Patienter i kontrollgruppen - NSAID och sjukgymnastik. Patienter observerades efter 1, 3, 6, 9 och 12 månader. Schemat för att använda läkemedlet Structum var klassiskt.
Patienternas kön, ålder, utbildning, artrosstadium, sjukdomsvaraktighet, smärtsyndrom, WOMAC, behov av NSAID, Lequesne-index samt direkta och indirekta kostnader för behandling av artros beaktades och analyserades.
Majoriteten av patienterna var medelålders människor, kvinnor (82-84%), personer med högre eller sekundär utbildning (för att skapa en gynnsam bakgrund för att uppnå ömsesidig förståelse med en läkare och efterlevnad). Sjukdomens varaktighet var ungefär jämförbar i experiment- och kontrollgrupperna. Skillnaden i kostnaden för ett års behandling för en patient med artros i grupperna var 125 dollar till förmån för den viktigaste.
Således är behandling med Structum under ett år mer lönsam än behandling med konventionella läkemedel, med hänsyn till merkostnaderna, vars källa är den otillräckliga kliniska effekten av NSAID, det vill säga frekventa förvärringar, komplikationer, biverkningar av läkemedelsbehandling. Structum gör det möjligt för patienten att behandlas effektivt och till en minimal kostnad.
 Motsvarande ledamot av Akademin för medicinska vetenskaper i Ukraina kompletterade professor V.N. Kovalenko anförandena från tidigare talare och delade data om en annan studie - utvärderade effektiviteten av kondroskyddande behandling hos patienter med gonartros baserat på 6-månaders uppföljning.
Motsvarande ledamot av Akademin för medicinska vetenskaper i Ukraina kompletterade professor V.N. Kovalenko anförandena från tidigare talare och delade data om en annan studie - utvärderade effektiviteten av kondroskyddande behandling hos patienter med gonartros baserat på 6-månaders uppföljning.
- Till skillnad från tidigare studier, för att övervaka det morfofunktionella tillståndet i brosk och andra komponenter i leden, utförde vi ultraljudundersökning av lederna i experiment- och kontrollgrupperna. Utvärdering av effektiviteten av användningen av läkemedlet baserades också på analysen av olika indikatorer, såsom WOMAC, Lequesne-index, bedömning av smärta i de drabbade lederna med den visuella analoga skalan (VAS) och andra. För alla dessa parametrar fick vi resultat som liknar de som presenterades vid dagens konferens, vilket återigen bevisar den höga standardiseringen av läkemedlet.
Ett inslag i vår studie var bedömningen av effektiviteten av Structum-användning enligt ultraljud av de drabbade lederna före och efter behandlingen. En minskning av ekogeniciteten i ledbrosket liksom en ökning av ledutrymmet, det vill säga regression av synovit och andra inflammatoriska-degenerativa förändringar i broskvävnaden, bevisades, vilket indikerar läkemedlets strukturmodifierande egenskaper.
Det är också anmärkningsvärt att den avslöjade signifikanta minskningen av ledutgjutning under 6 månader med kontinuerlig användning av Structum under hela denna period.
Dessutom studerade vi intensiteten i blodflödet i synoviet före och efter användning av läkemedlet kondroitinsulfat-4.6. Doppler-ultraljud gjorde det möjligt att dra slutsatsen att det fanns en signifikant förbättring av blodflödet i de drabbade lederna efter en behandling med Structum.
Således bekräftar studierna vid det ukrainska reumatologiska centret många analytiska och experimentella data för att bedöma Structums effektivitet och komplettera dem med resultaten av ovillkorligt objektiva forskningsmetoder (ultraljud inklusive Dopplersonografi). All data tyder på att Structum är ett läkemedel med strukturmodifierande egenskaper, har en kondroskyddande effekt och dess långvariga användning hos patienter med artros förbättrar objektivt och tillförlitligt de funktionella parametrarna i lederna, minskar belastningen av icke-steroida antiinflammatoriska och kortikosteroidläkemedel och har också gynnsamma ekonomiska parametrar i rationell användning.
För närvarande erövrar kondroskyddande läkemedel i allt högre grad läkemedelsmarknaden och man bör vara mycket försiktig när man väljer ett kvalitetsläkemedel. Kom ihåg följande för att göra detta.
- Cirka 13% av den aktiva substansen kondroitinsulfat kommer in i broskvävnaden. Därför bör den dagliga dosen kondroitinsulfat vara minst 1000 mg per dag. Följaktligen är preparat med doseringsformer av 100 mg eller mindre inte tillräckliga och försvårar långvarig administrering.
- Kondroitinsulfatberedningen bör framställas av säkra råvaror, för närvarande fjäderfäråvaror. Nötkreatursbaserade preparat kan vara bärare av prioninfektioner.
- Kondroprotektorer bör användas under lång tid med en gradvis minskning av dosen av NSAID, om möjligt - deras fullständiga avbrytande. Effekten förväntas tidigast två veckor efter början av användningen av kondroprotektorer.
- Eventuella kondroskyddande läkemedel kan bara vara effektiva i steg I - III i artros (enligt Kelgren), eftersom fullständigt förstört brosk inte kan återställas.
För närvarande är det mest lovande läkemedlet för behandling av artros fortfarande Structum, vilket uppfyller alla krav för effektivitet och säkerhet vid användning. Dess användning kan minska symtomen på inflammation och smärta, normalisera eller avsevärt förbättra de drabbade ledernas funktion, påverka metabolismen av brosk positivt, minska nedbrytningen och förstörelsen av ledvävnader och främja regression av den patologiska processen. Strukturapplikation är kliniskt effektiv, säker och kostnadseffektiv.
STATISTIK PÅ TEMA
20/01/2020 Osteoporos: från tidig diagnos till effektiv behandling
Osteoporos är en systemisk nedgång i skelettet, som kännetecknas av förändringar i massan och skadorna på cystvävnadens arkitektur, vilket kan leda till en minskning av risken för frakturer. För tidig upptäckt av patienter med hög risk för frakturer, liksom för inrättande av effektiva metoder för förebyggande och behandling av osteoporos, är det viktigt att känna till barnen till de gamla specialiteterna, vintern för första gången. För den viktigaste maten gavs respekt vid den internationella vetenskapliga och praktiska konferensen "Utvecklingen av cyst-språk-systemet och wik", som ägde rum den 21-22 juni 2019 i Kiev. ...
23.01.2020 Neurologi Upprätta diagnos och behandling av progressiva attacker
Progressiv ataxi är en grupp av barnsliga och vikbara neurologiska problem, som läkare inte ofta gifter sig med. Till din respekt presenteras en översikt över rekommendationerna för diagnostik och behandling av lägret, som har delats upp av en grupp patienter med hjälp av De Silva et al. i Storbritannien (Orphanet Journal of Rare Diseases, 2019; 14 (1): 51). Ataxi kan vara ett symptom på utbredd stagnation, men dynastin var fokuserad på den progressiva nedgången av Fridreichs ataxier, idiopatiska sporadiska cerebrala ataxier och specifika neurodegenerativa sjukdomar. ...
23.01.2020 Kardiologi Antitrombotisk terapi hos patienter på grund av icke-valvulär fibrillering av förmaket för en historia av akut koronarsyndrom och / eller tvärgående koronarinvolvering
Fibrillering av atrium (FP) är associerat med antagning till risken för dödsfall, sjukdom hos patienter med tromboembolisk acceleration, hjärtsvikt och sjukhusvistelse, funktionsstörning i dysfunktioner vid livöverföring, undernäring AF för bladlöss av uppskjuten kranskärlssyndrom (GCS), en utökad och vikbar klinisk situation som kräver antikoagulations- och trombocytbehandling (Kirchhof et al., 2016; Steffel et al., 2018) ....
23.01.2020 Neurologi Trance-metoder i praktiken av en psykoterapeut: en analytisk granskning
Nu har vår förståelse för trance förändrats, men inte mekanismen för dess förekomst. Det är vanligt att inkludera ett antal riktningar i trance-metoder i psykoterapi: förslag (förslag, hypnos), neurolingvistisk programmering (NLP), samt visualiseringsmetoden som kallas Leiners symboliska drama ...
Din webbläsare stöder inte JavaScript
För att visa webbplatsen helt, aktivera JavaScript i dina webbläsarinställningar!
I den nuvarande tidsåldern på Internet och skickligt presenterad information kan alla behöriga patienter berätta vad som är nödvändigt för att behandla leder: det är nödvändigt att återställa ledbrosket och det är nödvändigt att fylla på "smörjningen" av leden, dvs. intraartikulär vätska. Att ordinera läkemedel från gruppen kondroprotektorer verkar vara det bästa sättet att nå detta mål.
Den höga kostnaden för dessa läkemedel går utanför skalan, effekten av deras användning förväntas bli fantastisk. Men i verkligheten leder regelbundet intag av kondroskydd till patientens besvikelse. Vilka är dessa läkemedel? Och är de verkligen lika effektiva som marknadsföringsmaterialet lovar oss?
(chondros-brosk, protector-protector) - bokstavligen: ämnen som skyddar brosk (i synnerhet ledbrosk). Denna grupp läkemedel har dykt upp ganska nyligen. Den andra generationen av läkemedel har funnits i drygt tio år.
Beroende på utvecklingstiden, skiljer sig 3 generationer av kronoskyddande läkemedel:
1: a generationen (naturligt ursprung):
- av animaliskt ursprung (baserat på benmärg och broskvävnad hos djur och fisk) - Alflutop, Rumalon
- mucopolysackarider - Arteparon (Mukartrin)
2: a generationen(syntetiska monopreparat)
- baserat på kondroitinsulfat - Mukosat, Kondroxid, Structum, Khonsurid, Kondrolon, Kondrogard, Kondrosat, Artradol, Artiflex, Artrox, Arthrida, balsam "Toad Stone" (kosttillskott)
- baserat på glukosamin - Don, Artron Flex, Sustilak, Elbona, Sinart
III-generationen (komplexa syntetiska preparat som kombinerar kondroitinsulfat med glukosamin) - Teraflex, Artra, Artron Complex, Kondroitin-komplex, Formula-S, KONDRONOVA, Movex, Chondro-sila, Protekon, Inoltra (kosttillskott)
Kondroskyddare i kombination med icke-steroida antiinflammatoriska läkemedel utvecklas och produceras nu. Till exempel Teraflex Advance (en kombination av ibuprofen, glukosaminsulfat och kondroitinsulfat). Vissa forskare tillskriver kombinationer av kondroskydd med läkemedel från andra grupper till en ny, IV-generation.
Som en marknadsföringskamp för vissa kosttillskott av kondroskyddande typ, producerade i form av lösningar, används ibland namnet "kolloider". Även om namnet kolloider inte kännetecknar denna specifika grupp läkemedel, utan bara en av typerna av alla befintliga lösningar.
Separat bör markeras ersättare (proteser) av intraartikulär vätska - beredningar för intraartikulär administrering baserade på hyaluronsyra eller polymerer. Dessa är Ostenil, Sinvisk, Ortovisk, Gialgan, Gialual, Gyastat, Hyalurom, Giruan, Sinokrom, Suparts, Fermatron, Durolan, Coxartrum, ViskoPlus, Go-on, Euflexa, Hialubrix, Adant, Noltrex.
Utomlands kallas en grupp kondroskyddare SYSADOA (Symptomatiska långsamverkande drag av artros - symtomatiska långsamverkande läkemedel för artros)
Vad säger tillverkarna av kondroskydd?
Som tillverkarna anger, på grund av det faktum att kondroprotektorer innehåller komponenter i ledbrosk, som, när de intas, ingår i det skadade brosket och bidrar till dess förnyelse, de:
- bidra till att återställa vävnaden i ledbrosket och också skydda den från ytterligare förstörelse.
- de bidrar också till normaliseringen av både kvantiteten och kvaliteten på den intraartikulära (synoviala) vätskan.
Dessutom har de ingående substanserna i kondroprotektorer en måttlig antiinflammatorisk effekt som en ytterligare effekt.
Som ett resultat av denna effekt minskar patientens smärta, lederns funktion återställs och ledbrosket stärks.
Den terapeutiska effekten utvecklas efter långvarig användning av läkemedel. Vanligtvis minst efter 3 veckor och oftast efter 3-6 månader.
Det bör noterassom styrs av denna logik (för att fylla på de sjuka komponenterna i lederna med källor från utsidan), gör människor som har lidit av artros i många år ofta detta. De försöker äta gelékött, gelatin, bara ett avkok av frön. Och genom att jämföra jämförelsen till grotesken kan man komma ihåg att de nordamerikanska indianerna äter hjärtat av en besegrad fiende, men under en tidigare modig fiendes liv för att få sitt mod.
Och kondroprotektorer bör inte bara verka på ledbrosket utan också på hela kroppens brosk (inklusive örat, näsbrosk etc.).
Men kondroprotektorns måttliga antiinflammatoriska effekt bör ses närmare.
Långvarig praxis visar den kontroversiella effektiviteten hos kondroprotektorer
Men långsiktig praxis visar kontroversiell effektivitet grupper av läkemedel - kondroprotektorer. Vi möter regelbundet patienter som har tagit kondroprotektorer varje dag i flera år och inte har märkt någon terapeutisk effekt från dem. De fortsätter att ta dessa läkemedel, uppenbarligen på grund av tröghet och det kontinuerliga intensiva inflytandet av reklaminformation. Trots detta fortsätter de att ordineras allmänt av läkare och användas av patienter med led- och ryggradsproblem.
Den ursprungligen påstådda effekten av att återställa ledbrosk har ännu inte bekräftats. För att avgöra om restaureringen av ledbrosket har ägt rum är det tillräckligt att jämföra de vanliga röntgenbilderna av den sjuka leden, som tas före och efter behandling med kondroprotektorer. Fogutrymmets höjd indirekt indikerar tjockleken på ledbroskskiktet. Efter broskreparation bör sålunda höjden på fogutrymmet öka. Tyvärr har detta aldrig hänt förut. Fogutrymmets höjd förblir oförändrad eller minskar till och med.
I bästa fall observeras endast effekten av att skydda ledbrosket från ytterligare förstörelse under den tid då dessa läkemedel tas. Men han är också tveksam.
Det uppstår också många frågor biotillgänglighetolika former av droger. Vad är den verkliga mängden av den aktiva substansen som kommer in i den drabbade leden om läkemedlet inte injiceras direkt i leden, men tas oralt (i form av tabletter, pulver), i form av intramuskulära injektioner, och ännu mer i form av salvor. Uppenbarligen faller endast en symbolisk mängd medicin med sådana administreringsmetoder i det erforderliga området.
Varför är det ibland en positiv effekt när man tar kondroprotektorer?
Trots alla ovanstående omständigheter utvecklar en relativt liten andel av patienterna ibland en positiv effekt efter att ha tagit kondroprotektorer.
I den överväldigande majoriteten av fallen är detta patienter med milda stadier av sjukdomen. I avancerade fall av sjukdomar är effekten av kondroprotektorer nära noll.
Vad kan vara orsaken till denna förbättring hos vissa patienter om användningen av kondroskydd inte orsakar återställning av ledbrosket? Och om det inte finns några tydliga uppgifter om förbättringen av brosktillståndet till följd av att du tar kondroprotektorer? Den positiva effekten i dessa fall kan förklaras med inte kondroskyddande verkan utan antiinflammatorisk... Verkningsmekanismen för kondroprotektorer är associerad med stimuleringen av kondrocytfunktionen, en minskning av aktiviteten hos lysosomala enzymer (metalloproteinaser) och en ökning av kondrocyternas motstånd mot effekterna av proinflammatoriska cytokiner. De där. kondroprotektorer har samma effekt som icke-steroida antiinflammatoriska läkemedel (NSAID) - diklofenak, Movalis, Ortofen och många andra. Det är sant att den antiinflammatoriska effekten av kondroprotektorer är svagare än NSAID: s och utvecklas under lång tid.
Ja, långvarig användning av NSAID kan orsaka olika biverkningar (främst genom att påverka magslemhinnan). Men kondroskydd med långvarig användning (och de rekommenderas att tas under många månader) kan också orsaka biverkningar. En naturlig fråga uppstår: är det i det här fallet inte bättre att använda icke-steroida antiinflammatoriska läkemedel?
Låt oss till och med uttrycka en sådan "ramol" -tanke: det finns kanske ingen läkemedelsgrupp av kondroskyddare (i den meningen att det inte finns några läkemedel som "skyddar" ledbrosket)? Kanske de så kallade kondroprotektorerna bör klassificeras som antiinflammatoriska läkemedel med måttlig aktivitet? Då är icke-steroida antiinflammatoriska läkemedel (NSAID) mer aktiva antiinflammatoriska läkemedel. Och de mest aktiva är hormonella antiinflammatoriska läkemedel (glukokortikoider). I det här fallet faller allt på plats.
Det är inte för ingenting som de försöker inkludera icke-steroida antiinflammatoriska läkemedel (till exempel Teraflex Advance) i de mest moderna kondroprotektorerna. Farmaceuternas ansträngningar riktar sig inte till att skydda och "reparera" brosk, utan att stärka kampen mot inflammation.
Glöm inte heller det banala självhypnoseffektorsakas av en aggressiv reklamkampanj.
Det bör också komma ihåg att enligt rekommendationerna från utvecklarna av kondroskyddande läkemedel själva är det vettigt att ordinera dem endast i de inledande och mellersta stadierna av artros (I och II). I avancerade stadier (III och IV) finns det inga indikationer för utnämning av kondroskydd även enligt den officiella versionen.
Ojämn forskning
Här är bara några av uppgifterna från opartiska utländska studier som publicerats i auktoritativa publikationer i USA och Storbritannien:
- New England Journal of Medicine (2006): slutsats av en metastudie som utfördes på en grupp av 1583 patienter: kondroitinsulfat, glukosamin och någon kombination därav översteg inte effekten som erhölls med en konventionell placebo.
- American College of Physicians (2007): Storskaliga studier visar att den symptomatiska fördelen med kondroitin är minimal eller obefintlig. Användningen av kondroitin i rutinmässig klinisk praxis måste därför omprövas.
- BMJ: ledande allmän medicinsk tidskrift (2010): slutsatser baserade på 10 studier utförda på en grupp av 3803 patienter: jämfört med placebo, kondroitin och glukosamin och deras kombinationer visade ingen fördel.
Ett fundamentalt annorlunda tillvägagångssätt för gemensam behandling vid AKTA ® Arthroclinic
I AKTA ® Arthroclinic har länge övergivit användningen av kondroskydd. För behandling av leder används ett helt annat tillvägagångssätt, vilket har visat sin höga effektivitet under många års praxis.
Din webbläsare stöder inte videotaggen.
Artros är en av de vanligaste kroniska sjukdomarna, som enligt vissa uppskattningar drabbar en av fem personer 1. Dess konsekvenser är förödande för brosket som täcker lederna och benet under. Sprickor, erosion av benvävnad åtföljs av svår smärta och nedsatt rörlighet i leden, upp till en fullständig förlust av funktionalitet. Inte överraskande uppfattas framväxten av läkemedel som förmodligen kan reparera skadad vävnad som ett sugrör för en drunkning. Vilken typ av droger är det här och är mirakel verkligen värt att förvänta sig av dem?
NSAID: nackdelar med val av läkemedel
Under många decennier är icke-steroida antiinflammatoriska läkemedel (NSAID), som inkluderar diklofenak, ibuprofen, meloxikam och många andra, förstahandsbehandling för artros. Alla påverkar två patologiska länkar av sjukdomen - inflammation och smärta.
Samtidigt visar NSAIDs också oönskade reaktioner, varav det sorgliga ledarskapet tillhör gastropatier. En förvärring av magsårsjukdom, gastrit, buksmärta, halsbränna och andra gastrointestinala effekter är tyvärr ett av "telefonkort" för representanter för NSAID.
Dessutom påverkar läkemedel i denna grupp inte degenerativa processer i brosk och ben. De stoppar bara smärtsyndromet och minskar svårighetsgraden av den inflammatoriska reaktionen, medan leden fortsätter att kollapsa obevekligt.
Sådana betydande nackdelar tvingar både specialister och konsumenter att leta efter antingen ett alternativ till NSAID eller ett läkemedel som skulle öka effekten av antiinflammatorisk och smärtstillande behandling. Och på det post-sovjetiska territoriets territorium blev kondroprotektorer sådana droger.
Kondroprotektorns goda avsikter
Deras skillnad från NSAID är slående. För det första har de en mycket hög säkerhetsprofil på grund av att de är strukturella element i naturlig broskvävnad. De aktiva ingredienserna i moderna kondroprotektorer - kondroitinsulfat, glukosamin, kollagen - är en del av broskmatrisen. Tillsammans med detta påverkar kondroprotektorer, till skillnad från NSAID, orsaken till sjukdomen - dysfunktion hos broskceller, kondrocyter.
Verkningsmekanismen för kondroprotektorer, enligt bruksanvisningen, är mångfacetterad. Kondroskydd:
- aktivera kondrocyters arbete;
- undertrycka aktiviteten hos enzymer som förstör brosk;
- förhindra för tidig död av broskceller;
- undertrycka produktionen av ämnen som utlöser den inflammatoriska processen;
- förbättra mikrocirkulationen i benvävnad;
- minska smärtsyndrom.
Förutom en sådan imponerande lista ökar kondroprotektorer enligt vissa rapporter motståndet från broskvävnad mot den negativa effekten av NSAID och upprätthåller broskets elasticitet. Således representerar gruppen av kondroprotektorer:
- minska svårighetsgraden av symtom på artros - smärta, svullnad, nedsatt ledrörlighet;
- sakta ner utvecklingen av artros;
- kan kombineras med NSAID, så att du kan minska doserna och förbättra toleransen;
- har en hög säkerhetsprofil;
- visa en effekt även efter avslutad behandling.
Tre generationer
Inom den inhemska farmakologin skiljer sig flera generationer av kondroprotektorer:
- Första generationens preparat, till exempel ett bioaktivt koncentrat från små havsfiskar.
- Andra generationens läkemedel - hyaluronsyra, kollagen, glukosamin, kondroitinsulfat.
- Tredje generationens läkemedel är kombinationer av kondroprotektorer (till exempel glukosamin och kondroitin) eller kondroprotektorer med vitaminer, NSAID (diklofenak, ibuprofen) och andra aktiva ingredienser.
Utan undantag måste alla kondroskyddare tas under lång tid, under flera veckor eller till och med månader, och det rekommenderas att upprepa behandlingsförloppet flera gånger om året 2.
Kondroprotektorer presenteras på den inhemska marknaden i olika doseringsformer - tabletter, kapslar, pulver för oral administrering (dospåsar), injektioner, salvor, geler. Ett ganska brett spektrum och former av läkemedelsproduktion i denna grupp väcker logiska frågor från konsumenten: vilka läkemedel hjälper bättre? Finns det några av dem som kan förlänga ledens livslängd mest effektivt? De är inte lätta att svara på, och här är varför.
Vad säger evidensbaserad medicin?

Resultaten av stora kliniska studier bekräftar tyvärr inte de flesta egenskaper som tillverkarna hävdar. Endast ett fåtal studier visar en minskning av smärtsyndromet under långvarig behandling 3.
Observera att gruppen som kallas kondroprotektorer endast finns i OSS-länderna. Och i många länder, inklusive USA, är kondroitin och glukosamin inte ens registrerade som droger - de är kosttillskott.
En av de ledande organisationerna i världen som arbetar med artros, OARSI (Osteoarthritis Research International) rekommenderar inte användning av kondroitin och glukosamin för behandling av artros på grund av otillräckliga bevis. Även om vissa andra organisationer, såsom European Society for the Clinical and Economic Aspects of Osteoporosis and Osteoarthritis, fortfarande rekommenderar kondroitin och glukosamin 4.
Till förmån för användningen av dessa läkemedel stöds de främst av sin extremt goda tolerans och till och med en liten förmåga att lindra smärta. Kanske är det därför som kondroprotektorer inom hushållsmedicin fortfarande är ett av de mest använda läkemedlen, som har varit bland de mest sålda i många år.
Marina Pozdeeva
Foto depositphotos.com
-
 Intima-media-komplex: diagnostiskt värde Mer tät i intensitet
Intima-media-komplex: diagnostiskt värde Mer tät i intensitet
-
 Hur man behandlar blodkärl vid diabetes mellitus - kontraindikationer och rekommendationer Behandling av blodkärl i benen vid diabetes mellitus
Hur man behandlar blodkärl vid diabetes mellitus - kontraindikationer och rekommendationer Behandling av blodkärl i benen vid diabetes mellitus
-
 Tea tree eterisk olja: egenskaper, applikation, recensioner Tea tree oil från sprickor applikation
Tea tree eterisk olja: egenskaper, applikation, recensioner Tea tree oil från sprickor applikation
-
 Blodtransfusionskomplikationer
Blodtransfusionskomplikationer